Aplicación de-movimiento-didáctico-1
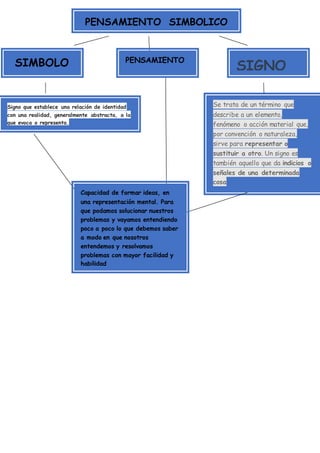
- 1. PENSAMIENTO SIMBOLICO SIMBOLO SIGNO Se trata de un término que describe a un elemento, fenómeno o acción material que, por convención o naturaleza, sirve para representar o sustituir a otro. Un signo es también aquello que da indicios o señales de una determinada cosa Signo que establece una relación de identidad con una realidad, generalmente abstracta, a la que evoca o representa. PENSAMIENTO Capacidad de formar ideas, en una representación mental. Para que podamos solucionar nuestros problemas y vayamos entendiendo poco a poco lo que debemos saber a modo en que nosotros entendemos y resolvamos problemas con mayor facilidad y habilidad
- 2. Aplicación de movimiento didáctico Primer nivel: Presentación y definición del problema Para esta unidad, se plantea el siguiente problema. TALLER: En los espacios que siguen se anotan los conceptos nuevos encontrados en la definición del problema. Luego se buscara y anotara la definición de cada uno. CONCEPTO DEFINICION Na0H Hidróxido de sodio Cantidad Número de unidades, tamaño o porción de una cosa, especialmente cuando es indeterminado. Cm3 Centímetros cúbicos H2S041M Ácido sulfúrico Neutralizar Hacer que disminuya o quede anulado el efecto de una acción o cosa mediante otra contraria que la contrarresta. Solución Mezcla de dos o más sustancias químicas TRAJO EN EQUIPO Se integran equipos de trabajo, con el fin de realizar las siguientes actividades: 1. Analizar el problema que acaba de planear, y relacionarlo con el tema de esta unidad pensamiento simbólico 2. Proponer por lo menos tres de investigación que ayuden a solucionar el problema planeado. ¿En dónde se aplica? ¿Para qué sirven las formulas? ¿Por qué se componen estas? Preguntas que pueden ser como guía Como una ayuda, se presentan a continuación algunas preguntas que pueden servir como guía para el trabajo de investigación que se realice Determinalacantidadde Na0H presente en100 cm3 de una solución,si parasu neutralizaciónse utilizan80cm3 de H2S04.1M
- 3. 1¿Que es neutralizar? = Es algo que de por concluido o anulado una acción o una cosa contraria a la otra. 2¿Por qué los ácidos y las bases se neutralizan? = Un ácido fuerte se neutraliza con una base fuerte, el pH experimenta una brusca variación justamente en el punto de equivalencia. 3¿Qué es una solución? = Es una respuesta eficaz o lógica sobre algún problema o algo 4¿Que significa NaOH H2SO4, .1M? = M=mol de soluto /Litro de solución sustituyendo los datos en la formula lo único que te hace falta es saber las moles de HCL H2SO4 o NaOH entonces los 0.25L de solución que tienes los pasas a multiplicar al otro lado de la ecuación así (0.25L)(1 M) = x moles de H2SO4 luego sacas el peso molecular del H2SO4 y lo multiplicas por 0.25 para saber cuántos gramos de H2SO4 están presentes y después tienes que saber la concentración del ácido que vas a usar para ver a cuantos ml de ese acido equivale la cantidad de gramos obtenida anteriormente con el NaOH como es sólido y no liquido lo puedes pesar en balanza seria (0.25L)(1M)=0.25 moles de NaOH después haces la operación (0.25mol)(40g/1 mol NaOH)= el número de gramos q te den es lo q necesitas para prepararla solución a 1M 5¿Qué sustancias se miden en centímetros cúbicos? = Los líquidos 6¿Los fluidos se miden en centímetros cúbicos? =si cualquier sustancia se podría medir así. 7, Si los ácidos y las bases en el estado líquido son fluidos. ¿Ácidos y bases se miden en centímetros cúbicos? = cualquier materia que sea fluido puede ser medido en unidades de volumen, es decir, centímetros cúbicos, litros, onzas, etc.
- 4. TABAJO EN PLENARIA En planearía, y con la coordinación del profesor, se realizaran las siguientes actividades 1. Cada equipo expondrá a las que llegaron a la actividad anterior 2. Se discutirá que preguntas de investigación están mejor planeadas 3. Se definirá la orientación que deben llevar a cabo para solucionar el problema planeado. Segundo nivel: Búsqueda,evaluación,análisis de información. TAREA 1. Se buscará en internet por lo menos tres fuentes cibergraficas de información para abordar el problema. Se enlistaran a continuación, con breve descripción de su contenido. Primera Fuente: Wikipedia. Elemento químico es un tipo de materia constituida por átomos de la misma clase. En su forma más simple, posee un número determinado de protones en su núcleo, haciéndolo pertenecer a una categoría única clasificada con el número atómico, aún cuando este pueda desplegar distintas masas atómicas. Es un átomo con características físicas únicas, aquella sustancia que no puede ser descompuesta mediante una reacción química. Segunda Fuente: definicion.de.com. denomina elemento químico a una sustancia que está formada por átomos del mismo tipo cuyos núcleos presentan la misma cantidad de protones más allá del número de neutrones. A la cantidad de protones que presenta cada átomo de un elemento químico se lo conoce como número atómico. Tercer Fuente: definicionabc.com. El de elemento químico es un concepto destacado dentro de la química justamente, que se usa para designar a aquella materia que se encuentra conformada por átomos que presenta igual clase.