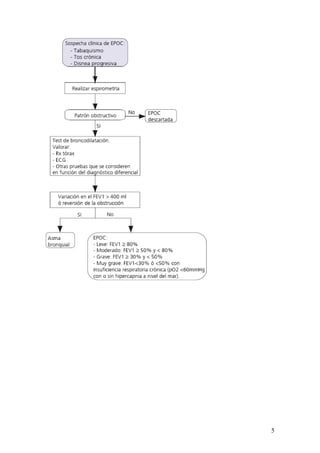
Este documento proporciona información sobre la enfermedad pulmonar obstructiva crónica (EPOC), incluida su definición, diagnóstico, evaluación inicial, diagnóstico diferencial, tratamiento de pacientes estables y situaciones especiales. Cubre temas como síntomas, espirometría, clasificación de gravedad, educación del paciente, vacunación, tratamiento farmacológico con broncodilatadores, corticoides y otros, y criterios para oxigenoterapia domiciliaria. El objetivo general del tratamiento es evitar la









![• Preparación quirúrgica: Aunque no existe un límite funcional que contraindique una
intervención, la presencia de EPOC grave constituye un factor de riesgo a tener en
cuenta en la evaluación prequirúrgica. En el paciente con EPOC, el lugar de la cirugía
es el factor predictor más importante para la presencia de complicaciones (mayor
riesgo en cirugía torácica y abdominal alta) y en ellos, la anestesia epidural tiene menor
riesgo que la general1
.
• Viajes: Si un paciente con EPOC planea un viaje, es importante recomendarle que lo
programe con anticipación. Si lo realiza en avión hay que considerar que la PO2
empeora durante el vuelo. En pacientes a tratamiento con oxigenoterapia domiciliaria,
hay que avisar a la compañía de vuelo de esta eventualidad, ya que aquellos con un
FEV1 <80% y pO2 <80 mmHg deberán recibir suplemento de O2 a 2 l/ min durante el
vuelo. Debe desaconsejarse los viajes en avión a los pacientes con EPOC en situación
inestable o que presenten bullas o quistes, por el riesgo de empeoramiento de su
cuadro y la posibilidad de desarrollar un neumotórax espontáneo 1,5,7
.
• Situación terminal: Teniendo en cuenta que la EPOC es una enfermedad progresiva,
es importante reconocer la fase terminal de la misma, para establecer los planes de
cuidados necesarios en este estadio (médicos, de enfermería, psicológicos, sociales y
familiares), de acuerdo con la familia y el paciente. La presencia de FEV1 <30%, IMC
<19 Kg/ m2, disnea severa, hipertensión pulmonar y exacerbaciones recurrentes que
requieran hospitalización, son hechos que nos deben hacer plantear su planificación
utilizando todos los recursos terapéuticos necesarios y disponibles 1,5,7
Bibliografía
1. Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the
diagnosis, management, and prevention of chronic obstructive pulmonary disease. Bethesda
(MD): Global Initiative for Chronic Obstructive Lung Disease, World Health Organization,
National Heart, Lung and Blood Institute; 2007 [NGC]
2. NICE. Chronic obstructive pulmonary disease: management of chronic obstructive pulmonary
disease in adults in primary and secondary care (NICE guideline). Clinical guideline 12
[Internet]. National Institute for Health and Clinical Excellence. [acceso 6/2/2009]. Disponible en:
http://www.nice.org.uk
3. Peces-Barba G, Barberà JA, Agustí A, Casanova C, Casas A, Izquierdo JL et al. [Diagnosis and
management of chronic obstructive pulmonary disease: joint guidelines of the Spanish Society
of Pulmonology and Thoracic Surgery (SEPAR) and the Latin American Thoracic Society
(ALAT)]Arch Bronconeumol. 2008 May;44(5):271-81. [PubMed] [Texto completo]
12](https://image.slidesharecdn.com/protocolodeepoc-140612034234-phpapp02/85/Barranquet-Protocolo-de-epoc-12-320.jpg)
![4. Rennard S I. Chronic obstructive pulmonary disease: Definition, clinical manifestations,
diagnosis, and staging. Uptodate; 2008 [acceso 18/6/2008]. Disponible en:
http://www.uptodate.com
5. CKS. Chronic obstructive pulmonary disease [Internet]. National Health Service; 2007. [acceso
6/2/2009]. Disponible en: http://cks.library.nhs.uk/
6. Celli BR, MacNee W; ATS/ERS Task Force. Standards for the diagnosis and treatment of
patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J. 2004 Jun;
23(6):932-46. [PubMed] [Texto completo]
7. Institute for Clinical Systems Improvement (ICSI). Chronic obstructive pulmonary disease.
Bloomington (MN): Institute for Clinical Systems Improvement (ICSI); 2007 Jan. [Texto
completo]
8. Currie G, Douglas JG. ABC of chronic obstructive pulmonary disease. Non-pharmacological
management BMJ 2006;332;1379-1381. [PubMed]
9. O'Donnell DE, Hernandez P, Kaplan A, Aaron S, Bourbeau J, Marciniuk D, et al. Canadian
Thoracic Society recommendations for management of chronic obstructive pulmonary disease -
2008 update - highlights for primary care. Can Respir J. 2008 Jan-Feb; 15 Suppl A:1A-8A.
[PubMed]
10. Ferguson GT, Make B. Management of stable chronic obstructive pulmonary disease. Uptodate;
2008 [acceso 6/2/2009]. Disponible en: http://www.uptodate.com
11. Peytremann-Bridevaux I, Staeger P, Bridevaux PO, Ghali WA, Burnand B. Effectiveness of
chronic obstructive pulmonary disease-management programs: systematic review and meta-
analysis. Am J Med. 2008 May; 121(5):433-443.e4. [PubMed]
12. Appleton S, Jones T, Poole P, Pilotto L, Adams R, Lasserson TJ, Smith B, Muhammad J.
Bromuro de ipratropio versus agonistas beta2 de acción prolongada para la enfermedad
pulmonar obstructiva crónica estable; 2006 (Revisión Cochrane traducida). En: La Biblioteca
Cochrane Plus, 2008 Número 1. Oxford: Update Software Ltd. [Resumen]
13. Duodecim Finnish Medical Society. Chronic obstructive pulmonary disease (COPD) [Internet].
En: EBM Guidelines. Evidence-Based Medicine [Internet]. Helsinki, Finland: Wiley Interscience.
John Wiley&Sons; 2005 [acceso 6/2/2009]. Disponible en: http://ebmg.wiley.com/ebmg/ltk.koti
14. Walters JAE, Walters EH, Wood-Baker R. Corticosteroides orales para la enfermedad pulmonar
obstructiva crónica estable; 2005 (Revisión Cochrane traducida). En: La Biblioteca Cochrane
Plus, 2008 Número 1. Oxford: Update Software Ltd. Disponible en: http://www.update-
software.com. (Traducida de The Cochrane Library, 2008 Issue 1. Chichester, UK: John Wiley
& Sons, Ltd.) [Resumen]
15. Poole PJ, Black PN. Agentes mucolíticos para la bronquitis crónica o la enfermedad pulmonar
obstructiva crónica; 2006 (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus,
2008 [Resumen]
16. American Thoracic Society and European Respiratory Society: Standards for de diagnosis and
management pf patients with COD. 2004 ATS/ERS Task Force.Standards for the diagnosis and
treatment of patients with COPD: a summary of theATS/ERS position paper. Eur Respir J. 2004
Jun;23(6):932-46 [PubMed]
17. Sánchez Agudo L, Cornudella R, Estopá Miró R, Molinos Martín L, Servera Pieras E. Indicación
y empleo de la oxigenoterapia continua domiciliaria. Arch Bronconeumol. 1998 Feb; 34(2):87-
94. [PubMed]
13](https://image.slidesharecdn.com/protocolodeepoc-140612034234-phpapp02/85/Barranquet-Protocolo-de-epoc-13-320.jpg)