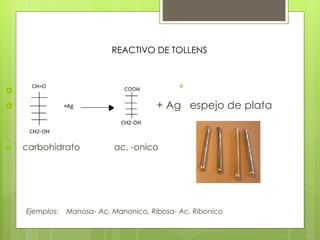
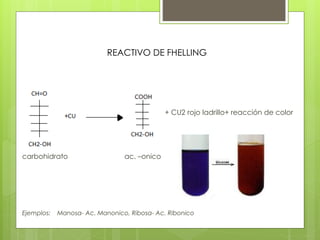
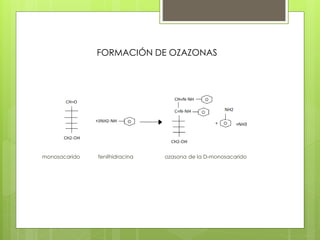
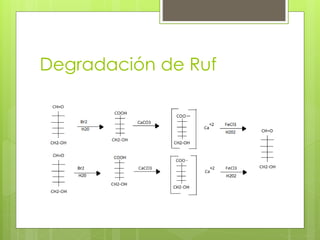
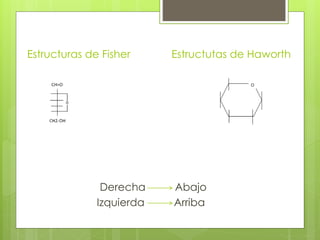
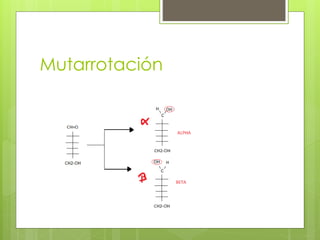
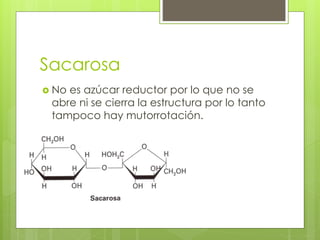
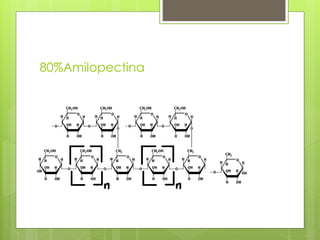
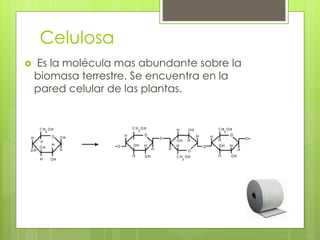
Este documento describe diversas reacciones químicas de compuestos orgánicos como alcanos, alquenos, alcoholes, aldehídos, cetonas y ácidos carboxílicos. También explica la estructura y tipos de carbohidratos como monosacáridos, disacáridos y polisacáridos, así como sus reacciones principales. Finalmente, detalla biopolímeros importantes como el almidón, glucógeno, celulosa y quitina que cumplen funciones de almacenamiento y estructura