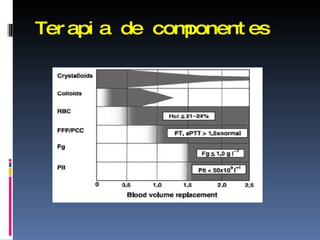
Este documento describe el concepto de control de daño en trauma, el cual involucra una intervención estructurada desde la sala de emergencias hasta la UCI para evitar hipotermia, acidosis y coagulopatía que puedan empeorar el sangrado. Esto incluye transfusiones tempranas de componentes sanguíneos, resucitación hipotensiva y corrección de factores de riesgo como hipocalcemia, con el fin de estabilizar al paciente para una posterior cirugía de reparo definitivo de lesiones. El control de daño ha mejorado los resultados en