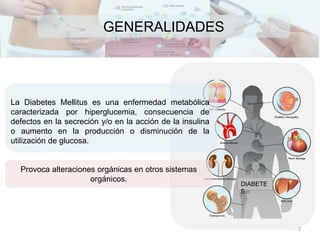
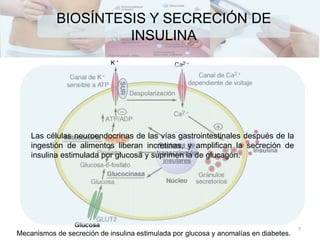
Existen varios tipos de diabetes mellitus que resultan de la interacción entre factores genéticos y ambientales. La diabetes tipo 1 se caracteriza por la destrucción de las células beta pancreáticas que producen insulina, mientras que la diabetes tipo 2 generalmente involucra resistencia a la insulina. El diagnóstico se basa en los niveles de glucosa en sangre y otros exámenes. El tratamiento busca controlar los niveles de glucosa a través de la dieta, ejercicio y medicamentos como la insulina.




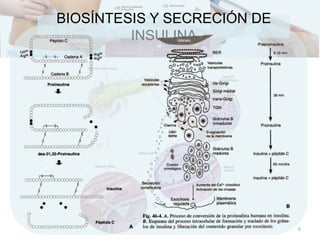
![ACCIÓN DE LA INSULINA
En el ayuno
[ ] bajas de insulina
Aumenta la producción de glucosa
Gluconeogénesis, glucogenólisis.
Disminuye la captación de glucosa.
8](https://image.slidesharecdn.com/diabetes-150222100437-conversion-gate01/85/DIABETES-8-320.jpg)









![Mayor masa
de adipocitos
[ ] Ag circulantes
libres y otros
productos de los
adipocitos
Regulan: peso,
apetito y gasto de
energía y sensibilidad
a la insulina
Resistencia a
la insulina
Liquido dentro de miocitos de
musculo estriado
Insulin
a
Fosforilación oxidativa
mitocondrial y aminora la
producción de ATP
mitocondrial
Peróxidos
de lípido
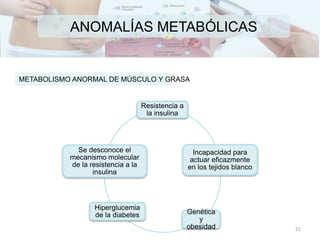
ANOMALÍAS METABÓLICAS
METABOLISMO ANORMAL DE MÚSCULO Y GRASA
22](https://image.slidesharecdn.com/diabetes-150222100437-conversion-gate01/85/DIABETES-22-320.jpg)