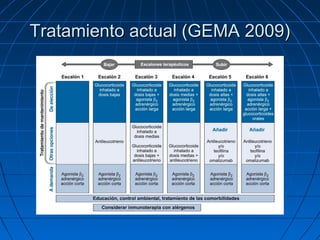
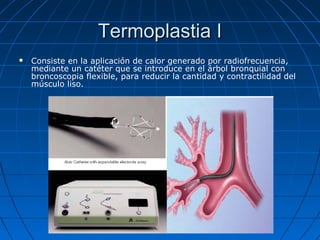
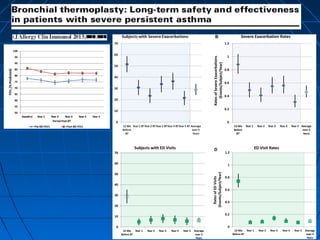
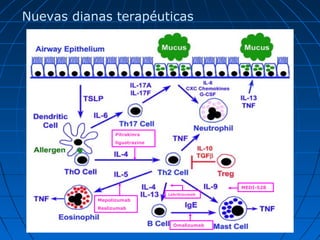
Este documento describe futuros tratamientos para el asma, incluyendo nuevos fármacos biológicos dirigidos a citoquinas e inflamación. Se discuten anticuerpos monoclonales contra IL-5, IL-13, IL-4, IL-9 y TNF-alfa, los cuales han demostrado reducir síntomas y exacerbaciones en algunos pacientes graves. También se mencionan nuevos broncodilatadores de larga duración, modificadores de la vía del ácido araquidónico y anticolinérgicos como potenciales terapias adic