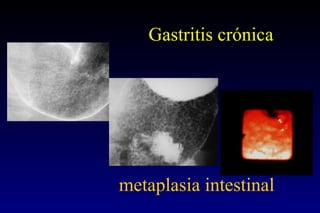
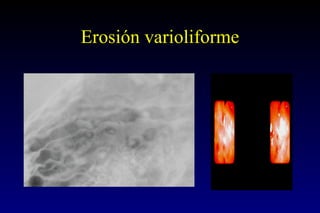
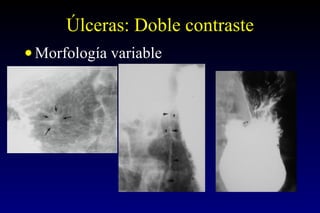
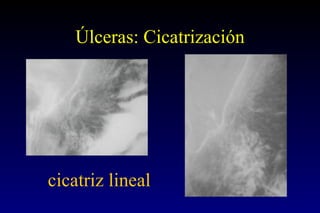
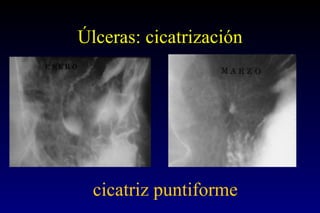
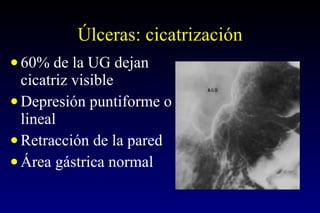
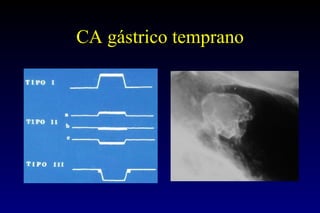
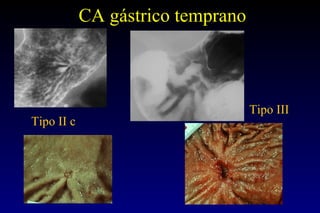
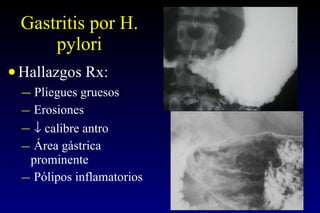
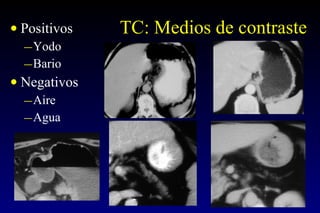
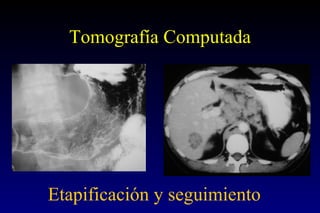
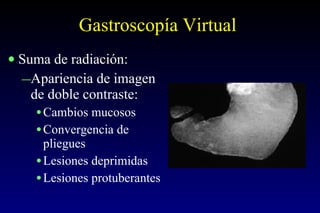
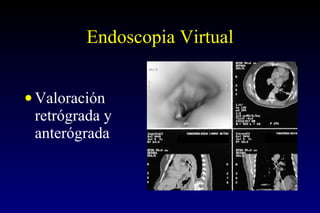
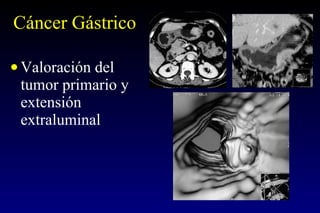
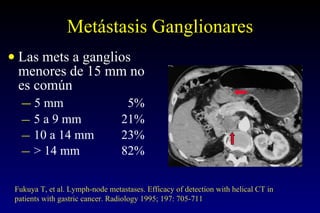
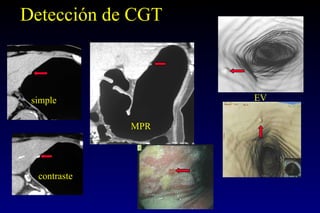
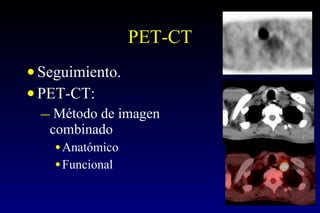
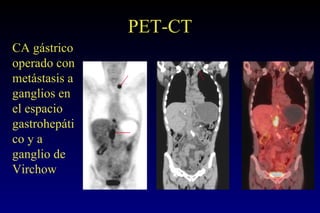
Este documento describe la historia y el desarrollo de la radiología del estómago, incluidas las técnicas de imagen como la radiografía simple, la tomografía computarizada multidetector (TCMD) y la tomografía por emisión de positrones (PET). La TCMD proporciona una estadificación precisa del cáncer gástrico en comparación con otros métodos como la endoscopia y la ultrasonografía endoscópica. La PET-CT es útil para el seguimiento de la respuesta al tratamiento y la detección de recidivas en