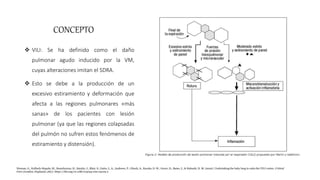
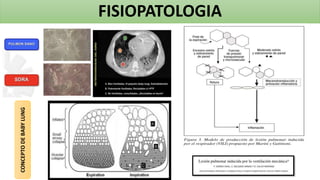
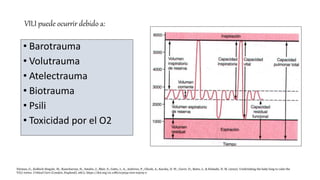
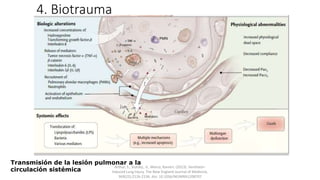
Este documento trata sobre la lesión pulmonar inducida por ventilación mecánica (VILI). Explica que el VILI puede ocurrir debido a fenómenos como el barotrauma, volutrauma, atelectrauma y biotrauma. También describe los mecanismos fisiopatológicos subyacentes como el estrés y la deformación pulmonar, y las manifestaciones clínicas como neumotórax. El documento analiza los efectos de las estrategias de ventilación protectora en pacientes con síndrome de