Tema 5. Citología Ginecológica
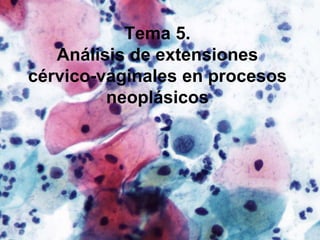
- 1. Tema 5. Análisis de extensiones cérvico-vaginales en procesos neoplásicos
- 2. 1. Alteraciones morfológicas de la infección por VPH. Lesiones histológicas y citología • El VPH es el virus del papiloma humano que se transmite de forma venérea y está relacionado con el cáncer de cérvix. Este virus produce una lesión intraepitelial que suele localizarse en el límite escamo-columnar o zona de transformación. • Una vez que el virus produce la infección puede permanecer sin replicarse, dando lugar a una infección latente, sin cambios morfológicos y sin capacidad infectiva. Otras veces, el virus entra en el núcleo de la célula infectada y se replica, produciendo modificaciones citopáticas, contagio por transmisión sexual e incluso progresión al cáncer. • En la actualidad se han identificado más de 100 tipos de VPH y dentro de los que afectan a la mucosa genital se distinguen tres grandes grupos: – Bajo riesgo oncogénico: se han encontrado preferentemente en lesiones benignas y sólo ocasionalmente en carcinomas. Los más comunes son el 6 y el 11. – Medio riesgo oncogénico: el 31 y el 33 son los más comunes. – Alto riesgo oncogénico: se encuentran en lesiones intraepitaliales de alto riesgo y en los carcinomas. Los más frecuentes son el 16 y el 18.
- 3. • Existe un cambio citopático muy característico del VPH en las células escamosas cervicales denominado coilocito. Es una célula escamosa madura con una cavitación perinuclear de límites muy netos, que deja un citoplasma reducido a un anillo externo denso. A esto se unen alteraciones nucleares: bi- multinucleación, núcleos aumentados, irregulares, de diferentes tamaños, hipercromáticos y con ausencia de nucléolo. • La lesión escamosa intraepitelial de bajo grado (LSIL) es generalmente una infección transitoria por VPH, mientras que la lesión escamosa intraepitelial de alto grado (HSIL) se asocia más a la persistencia viral y a un mayor grado de progresión, correspondiendo, por lo tanto, a verdaderos cambios malignos.
- 4. 2. Lesiones preneoplásicas. Clasificaciones • 2.1. Sistema Bethesda. El fin principal de este sistema es comunicar al médico solicitante la mayor información posible para ser utilizada en el manejo de la paciente, a través de un informe descriptivo en el que se incluyan todos los aspectos citológicos (a nivel hormonal, morfológico y microbiológico). La terminología usada en el Sistema Bethesda 2001 es la siguiente: – Tipo de muestra: citología convencional, líquida u otro tipo de muestra. – Calidad de la muestra: • Satisfactoria para la evaluación: presencia o no de células endocervicales (zona de transformación). • Satisfactoria para la evaluación pero limitada por diversas razones. • Insatisfactoria para la evaluación. – Clasificación general: • Negativo para malignidad o lesión intraepitelial: – Organismos: » Trichomonas vaginalis. » Organismos micóticos morfológicamente consistentes con cándida. » Cambios en la flora sugestiva de vaginosis bacteriana. » Bacterias morfológicamente consistentes con actinomyces. » Cambios celulares consistentes con herpes simplex virus.
- 5. – Cambios celulares reactivos asociados: » Inflamación (incluye reparación típica). » Radiación. » DIU. » Estado de células glandulares posthisterectomía. » Atrofia. – Otros hallazgos no neoplásicos (células endometriales en mujer mayor de 40 años). – Otras. • Anomalías en células epiteliales: – Células escamosas: » Células escamosas atípicas (ASC): de significado indeterminado (ASCUS) o de significado incierto, por lo que no se puede descartar HSIL (ASCH). » LSIL (lesión escamosa intraepitelial de bajo grado). » HSIL (lesión escamosa intraepitelial de alto grado). » Carcinoma epidermoide. – Células glandulares: » AGUS (células glandulares atípicas de significado incierto); endocervicales o endometriales. » Células glandulares endocervicales que favorecen neoplasia. » Adenocarcinoma endocervical in situ (AIS). » Adenocarcinoma endocervical, endometrial, extrauterino o sin especificar (NOS). • Otras neoplasias malignas. – Resultados.
- 6. Células ASCUS (atipia de significado incierto).
- 7. Lesión intraepitelial escamosa de bajo grado (LSIL). Núcleos con halos claros alrededor, irregularidades en el contorno, morfología típica HPV.
- 8. Adenocarcinoma in situ (AIS) en cuello de útero. Estructuras rosetoides (glándulas neoplásicas). Tinción de Papanicolaou .
- 9. • 2.2. Relaciones entre las distintas clasificaciones. – Sistema displasia-carcinoma in situ. En 1949, Papanicolau introduce los términos de displasia en biopsias, y de discariosis en citología, para designar cambios preneoplásicos. La mayoría de estas lesiones, dejadas a su evolución, regresan o permanecen inalteradas por mucho tiempo. En 1961, en el Primer Congreso Internacional de Citología celebrado en Viena, se acuerda que los términos para las lesiones cervicales sean: carcinoma invasor, carcinoma in situ (CIS) y displasia. La displasia se gradaba como leve, moderada y severa o grave, a las que habría que añadir el CIS ya definido. La clasificación se usaba tanto en biopsia como en citología. – Neoplasia intraepitelial cervical (NIC-CIN). En 1967 se propone el término de neoplasia intraepitelial cervical (NIC-CIN) con tres grados progresivos (1, 2, 3), incluyéndose en el grado 3 tanto la displasia grave como el CIS. Esta clasificación fue usada durante más de 20 años internacionalmente. – Lesión intraepitelial escamosa (alto-bajo grado). Representantes de organismos internacionales, científicos y profesionales liderados por el Instituto Nacional del Cáncer de Estados Unidos en Bethesda (Maryland) decidieron el sistema de nomenclatura para informes citológicos ginecológicos (sistema o clasificación Bethesda), en el que se unificaron criterios y se adoptaron recomendaciones que la experiencia general acumulada aconsejaban. El término “alto grado” de Bethesda incluye en CIN 2 y CIN 3 de la clasificación de Richardt, y el término “bajo grado” incluye en CIN 1 y las alteraciones celulares producidas por VPH.
- 10. 3. Anomalías de las células epiteliales escamosas • Importante: sólo las células bien conservadas deben evaluarse para llegar a un diagnóstico concreto. El diagnóstico de malignidad se basa en un conjunto de alteraciones morfológicas atípicas del frotis completo, que se dividen en: alteraciones del citoplasma, alteraciones del núcleo, células escamosas atípicas de significado incierto (ASC), lesión intraepitelial escamosa de bajo grado (LSIL), de alto grado (HSIL), y carcinoma escamoso infiltrante.
- 11. • 3.1. Alteraciones del citoplasma. Por sí solas no constituyen un signo de malignidad, pero tienen que coexistir con las alteraciones nucleares. – Pleomorfismo: distintas formas (raqueta, renacuajo, etc.). – Vacuolización: estructuras esféricas y transparentes en el interior del citoplasma. Pleomorfismo en el citoplasma de células en carcinoma escamoso. Núcleos hipercromáticos “en tinta china”. Grupos de células escamosas tipo metaplasia con características atípicas, algunas con el citoplasma vacuolado, con núcleo algo agrandado y nucléolo evidente.
- 12. • 3.2. Alteraciones del núcleo. Las más importantes son: – Multinucleación: más de un núcleo en el mismo citoplasma. – Anisonucleosis: diferentes tamaños de los núcleos. – Polimorfismo: distintas formas (alargados, fusiformes, etc.). – Hipercromasia: núcleos con abundante ADN que se tiñen muy oscuros. – Cambios en el patrón cromatínico: la cromatina se agrupa en grumos gruesos, densos e hipercromáticos, que dejan áreas claras. – Irregularidades en la membrana nuclear: consisten en dobleces, angulaciones, aumento del grosor, etc. – Nucléolos: aumento del tamaño y del número. – Cambios en la relación núcleo/citoplasma: los núcleos neoplásicos son mayores que los de las células normales.
- 13. • 3.3. Células escamosas atípicas de significado incierto (ASC). ASC son las siglas en inglés de células escamosas atípicas de significado incierto, terminología que se utiliza en el diagnóstico citológico cuando existe atipia celular que, cuantitativa y/o cualitativamente, es insuficiente para la lesión intraepitelial. Dentro del epígrafe ASC, la clasificación Bethesda distingue dos apartados con los siguientes criterios diagnósticos: – ASCUS: cuando las alteraciones celulares sugieren, aunque insuficiente, una lesión intraepitelial baja (LSIL). – ASCH: no se puede descartar HSIL porque se identifican alteraciones típicas de alto grado, pero son escasas las células afectadas.
- 14. ASC-US 1 – binucleated cells, mild nuclear hyperchromia and low N and C ratio. ASC-H 1 – cells appear similar to HSIL.
- 15. • 3.4. Lesión intraepitelial escamosa de bajo grado (LSIL). Esta lesión precancerígena sólo afecta al tercio basal del epitelio escamoso y puede progresar a un carcinoma infiltrante, permanecer estable o regresar/involucionar (espontáneamente o después de un tratamiento). Comprende los cambios celulares de la displasia leve y los patognomónicos (síntomas que aparecen únicamente en el marco de una enfermedad específica) de la infección por VPH. – Displasia leve. Son células escamosas superficiales e intermedias, generalmente aisladas o en grupos poco cohesivos. Las alteraciones nucleares son moderadas: aumento del tamaño nuclear (3 veces mayor) con el lógico aumento de la relación núcleo/citoplasma, hipercromatismo, bi o multinucleación, núcleo con bordes angulados y nucléolos pequeños o ausentes. – Efecto citopático por VPH: • Coilocitos. Células maduras con cavitación perinuclear traslúcida y bordes bien marcados, rodeadas por un citoplasma denso bien definido y con las alteraciones nucleares anteriormente descritas. • Paraqueratosis. Consiste en la queratinización anómala de las células escamosas. Son células de pequeño tamaño, con citoplasma muy orangófilo y núcleos picnóticos con atipia. Suelen disponerse en grupos tridimensionales aunque también de forma aislada.
- 16. A. Parakeratosis: 1 – orange, keratinizing cytoplasma; 2 – small nuclei with an increased chromatin concentration (pyknotic nuclei). B. Hyperkeratosis: keratized-anucleated cells.
- 17. LSIL 1 – enlarged nuclei (approximately 5 x intermediate cell nucleus); 2 – multinucleated cells; 3 – irregular nuclear margins; 4 – presence of rough chromatin deposits; 5 – presence of koilocytes.
- 18. • 3.5. Lesión intraepitelial escamosa de alto grado (HSIL). La afectación supera los 2/3 inferiores del epitelio, produciendo un trastorno total de la maduración de la mucosa. Incluye la displasia moderada y severa o carcinoma in situ (cuando no exista rotura de la membrana basal y, por lo tanto, no infiltre al estroma). En la citología se observan células inmaduras (basales y parabasales) de forma aislada, en placas no cohesivas o, raramente, en agregados de aspecto sincitial. Presentan escaso citoplasma, mayor variación en la forma y tamaño de los núcleos y la alteración de la relación núcleo/citoplasma es mayor que en la displasia leve. Existe mayor hipercromatismo, una membrana nuclear irregular y los nucléolos siguen siendo ausentes.
- 19. HSIL 1 – increased number of parabasal cells, enlarged nuclei, irregular nuclear margins, expressed hyperchromia and the presence of rough chromatin deposits.
- 20. • 3.6. Carcinoma escamoso infiltrante. Los carcinomas epidermoides se clasifican en: – Carcinoma epidermoide in situ (no infiltra el estroma cervical). – Carcinoma epidermoide microinvasivo (infiltra hasta un límite de 5 mm de profundidad y menos de 7 mm de extensión lateral). – Carcinoma epidermoide infiltrante (puede ser no queratinizante o queratinizante).
- 21. El carcinoma escamoso invasivo de cérvix es precedido por cambios pretumorales que corresponden a lesiones escamosas intraepiteliales (SIL). El carcinoma epidermoide constituye el 90% de los tumores y, en ocasiones, da lugar a un diagnóstico citológico difícil por los restos necróticos y hemorrágicos, así como por los cambios degenerativos en las células neoplásicas. Las extensiones citológicas de carcinoma epidermoide infiltrante presentan: – Citoarquitectura: células escamosas poco cohesivas. – Citoplasmas: son densos, bien definidos y sin vacuolas. Además, los carcinomas queratinizantes presentan rasgos de diferenciación citoplasmáticos y extracelular, producto de una queratinización anormal que no indica malignidad: • Orangofilia: células anarajandas con apariencia hialina y refringente. • Células alargadas: célula fusiforme y fina con núcleo picnótico denominada “célula en fibra” y célula con un extremo redondeado donde se encuentra el núcleo y una prolongación citoplasmática alargada, llamada célula en renacuajo. • Anillos citoplasmáticos: sucesivas líneas concéntricas de queratinización en el citoplasma. • Perlas córneas: remolinos concéntricos de células escamosas de pequeño tamaño y núcleos picnóticos. • Acúmulos eosinófilos: estructuras esféricas de queratina. – Núcleo: gran aumento del tamaño del núcleo y de la relación núcleo/citoplasma. Además, hay variación de la forma del núcleo, con frecuentes escotaduras y angulaciones, y los nucléolos están ausentes. • Carcinomas bien diferenciados: son los más comunes y presentan núcleos hipercromáticos denominados “en tinta china”. • Carcinomas pobremente diferenciados: tienen una membrana nuclear con engrosamiento irregular y cromatina en grumos con espacios claros, parecida a la de los adenocarcinomas. – Fondo:compuesto por restos de sangre, fibrina y fragmentos celulares que forman un típico fondo sucio, denominado diátesis tumoral, que constituye un criterio de invasión.
- 22. Squamous cell carcinoma 1 – signs of HSIL; 2 – large nuclei and irregular chromatin deposits; 3 – tumor diathesis; 4 – cellular polymorphism.
- 23. 4. Anomalías de las células epiteliales glandulares • 4.1. Células glandulares atípicas de significado incierto (AGUS). Se utiliza este término cuando observamos células glandulares con alteraciones citológicas que sugieren un adenocarcinoma, pero faltan criterios cualitativos y cuantitativos para afirmarlo con seguridad. Es recomendable diferenciar el origen endocervical del endometrial, pero en la práctica es muy difícil. Atypical glandular cells: AGUS 1 – endocervical (glandular) cells arranged in piles, hyperchromasia. 1
- 24. • 4.2. Adenocarcinoma endocarvical. – Adenocarcinoma in situ (AIS). • Citoarquitectura: células agrupadas con amontonamiento y superposición, que frecuentemente se observan en grupos en empalizada con núcleos protuyendo en los bordes, denominados “en plumaje”, o también en forma de roseta. • Citoplasma: escaso, con bordes mal definidos y espumosos o vacuolados. • Núcleo: escasa atipia nuclear, hipercromasia, escaso nucléolo, moldeamiento nuclear y presencia de cuerpos apoptóticos y mitosis. • Fondo: limpio o inflamatorio, sin diátesis tumoral (predisposición orgánica a convertirse en tumor), debido a la inexistencia de invasión estromal.
- 25. Adenocarcinoma in situ – AIS A characteristic arrangement of cells in a “rosette-shaped-pattern” is common; increased N and C ratio; nuclei appear oval-shaped; irreglar chromatin deposits “Salt-Pepper”; mucosal cells are diversified.
- 26. – Adenocarcinoma invasivo. • Citoarquitectura: grandes grupos cohesivos, tridimensionales y con superposición, que a veces presentan formaciones papilaroides. • Citoplasma: escaso, con bordes mal definidos y espumosos. • Núcleo: grande, con una alta relación núcleo/citoplasma. Cromatina irregular glandular con aclaramiento paracromático y macronucléolo. • Fondo: con diátesis tumoral. – Adenocarcinoma endometrial. • Citoarquitectura: pequeños grupos muy cohesivos, generalmente en forma de roseta, con neutrófilos fagocitados en su interior. • Citoplasma: muy escaso, con vacuolas citoplasmáticas. • Núcleo: leve aumento e irregularidad del núcleo y nucléolo presente. • Fondo: sucio, con restos celulares.
- 27. Adenocarcinoma 1 – round and large nuclei; increased cellular cytoplasma; 2 – macronucleoli are common; 3 – tumor diathesis.
- 28. Adenocarcinoma endometrial grado III: invadiendo más de la mitad del músculo uterino. Adenocarcinoma endometrial (corte histológico teñido con H-E).