PANCREATITIS AGUDA (3) [Autoguardado].pptx
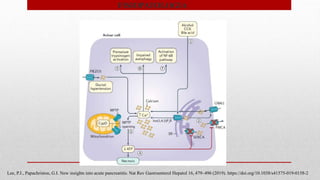
- 1. Lee, P.J., Papachristou, G.I. New insights into acute pancreatitis. Nat Rev Gastroenterol Hepatol 16, 479–496 (2019). https://doi.org/10.1038/s41575-019-0158-2 • FISIOPATOLOGIA
- 2. Lee, P.J., Papachristou, G.I. New insights into acute pancreatitis. Nat Rev Gastroenterol Hepatol 16, 479–496 (2019). https://doi.org/10.1038/s41575-019-0158-2
- 3. Lee, P.J., Papachristou, G.I. New insights into acute pancreatitis. Nat Rev Gastroenterol Hepatol 16, 479–496 (2019). https://doi.org/10.1038/s41575-019-0158-2
- 4. Pancreatitis Aguda • FISIOPATOLOGIA Señalización del calcio Activación prematura del tripsinogeno Estrés del retículo endoplásmico, respuesta proteica desplegada y autofagia Necrosis celular y liberación de DAMP´s Producción de NF-kappa beta Disfunción mitocondrial, autodigestión de páncreas y tejidos circundantes
- 6. Pancreatitis Aguda • DIAGNOSTICO Clínico Dolor abdominal Súbito Transfictivo Hemicinturón Otros síntomas Náuseas y vómito Distención abdominal Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 7. Pancreatitis Aguda • DIAGNOSTICO Laboratorios Amilasa Elevación x3 6-12 hrs 35-50% saliva Lipasa Sensibilidad 85-100% Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 8. Pancreatitis Aguda • DIAGNOSTICO Imagen Ultrasonido Anatómicos Tomografía Hemorragia activa RM Necrosis hemorrágica Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 9. Pancreatitis Aguda • DIAGNOSTICO • Se basa en el cumplimiento de 2 de 3 de los siguientes criterios: 1. Clínico. 2. Laboratorio. 3. Imagen. Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 10. • PUNTOS PANCREÁTICOS Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 11. Pancreatitis Aguda • LABORATORIO • Proteína C Reactiva >150 mg/l al tercer día como factor pronóstico de severidad. • Hematocrito >44% representa un factor de riesgo independiente de necrosis pancreática. • Urea >20 mg/dl predictor independiente de mortalidad. • Procalcitonina sensible para detectar infección pancreática, cifras bajas fuerte predictor negativo de necrosis infecciosa. • En ausencia de litiasis y alcoholismo, una determinación de triglicéridos superior a 1000 mg/dl orienta a la etiología Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN, Crockett S, et al. American gastroenterological association institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018;154(4):1096–101. http://dx.doi.org/10.1053/j.gastro.2018.01.032
- 13. Clasificación Grados de severidad Predicción de severidad Pronóstico Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 14. Pancreatitis Aguda • SEVERIDAD 1974 • CRITERIOS DE RANSON Sensibilidad 63% Especificidad 76%. 0-2 puntos – 0.9% 3-4 puntos – 16% 5-6 puntos – 40% 7-8 puntos – 100% Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 15. Pancreatitis Aguda • SEVERIDAD 1984 • CRITERIOS DE GLASGOW Sensibilidad 72% Especificidad 84% Una puntuación ≥ 3 predice pancreatitis aguda severa Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 16. Pancreatitis Aguda • MORTALIDAD 2008 • ESCALA BISAP Sensibilidad 17.5% Especificidad 94% Puntuación de 3 o mas, predice pancreatitis severa. Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 17. Pancreatitis Aguda • MORTALIDAD 1985 • CRITERIOS APACHE 0-4 4 5-9 8 10-14 15 15-19 25 20-24 40 25-29 55 30-34 75 >34 85 Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 18. Pancreatitis Aguda • SEVERIDAD 1995- 2013 • CRITERIOS DE ATLANTA Leppäniemi, A., Tolonen, M., Tarasconi, A. et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg 14, 27 (2019). https://doi.org/10.1186/s13017-019-0247-0
- 19. Pancreatitis Aguda • SEVERIDAD 2013 • DETERMINANTES Leppäniemi, A., Tolonen, M., Tarasconi, A. et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg 14, 27 (2019). https://doi.org/10.1186/s13017-019-0247-0
- 20. Pancreatitis Aguda • CLASIFICACIÓN REVISADA DE ATLANTA • Pancreatitis leve • Sin falla orgánica • Sin complicaciones locales/sistémicas Pancreatitis moderadamente severa • Falla orgánica transitoria (<48 hrs) • Complicaciones locales o sistémicas sin persistencia de falla orgánica • Pancreatitis Severa • Falla orgánica simple o múltiple persistente (>48 hrs) • CLASIFICACIÓN BASADA POR DETERMINANTES • Pancreatitis leve • No falla orgánica y no necrosis pancreática • Pancreatitis moderada • Falla orgánica transitoria y/o necrosis (peri)pancreática estéril • Pancreatitis Severa • Falla orgánica persistente o necrosis (peri)pancreática infectada • Pancreatitis crítica • Falla orgánica persistente y necrosis (peri)pancreática infectada Leppäniemi, A., Tolonen, M., Tarasconi, A. et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg 14, 27 (2019). https://doi.org/10.1186/s13017-019-0247-0
- 21. Pancreatitis Aguda • CLASIFICACION POR IMAGEN Índice de Morbilidad Mortalidad Severidad
- 22. Pancreatitis Aguda • CLASIFICACION POR IMAGEN Leppäniemi, A., Tolonen, M., Tarasconi, A. et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg 14, 27 (2019). https://doi.org/10.1186/s13017-019-0247-0
- 23. Tratamiento Analgesia Fluidoterapia Apoyo nutricional temprano Leppäniemi, A., Tolonen, M., Tarasconi, A. et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg 14, 27 (2019). https://doi.org/10.1186/s13017-019-0247-0
- 24. Pancreatitis Aguda • TRATAMIENTO • FLUIDOTERAPIA Ringer Lactato para la reanimación inicial del fluido en la pancreatitis aguda, de 5 a 10 ml/ kg/ h. El enfoque preferido para evaluar la respuesta a la reanimación con líquidos debe basarse en una o más de las siguientes: 1) Objetivos clínicos no invasivos. 2) Objetivos clínicos invasivos. 3) Objetivos bioquímicos. Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN, Crockett S, et al. American gastroenterological association institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018;154(4):1096–101. http://dx.doi.org/10.1053/j.gastro.2018.01.032
- 25. Pancreatitis Aguda • TRATAMIENTO • NUTRICIÓN EN LA PANCREATITIS AGUDA • En pancreatitis leve, se recomienda iniciar alimentación oral si no hay náuseas y vómitos, ni dolor abdominal. • En pancreatitis severa, se recomienda nutrición parenteral para prevenir complicaciones infecciosas, iniciar alimentación oral en cuanto disminuya el vómito. Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN, Crockett S, et al. American gastroenterological association institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018;154(4):1096–101. http://dx.doi.org/10.1053/j.gastro.2018.01.032
- 26. Pancreatitis Aguda • Analgesia • Principal meta, utilizar los medicamentos necesarios y las vías (intravenoso, epidural, multimodal) • AINE´s, Opioides y anestésicos locales • Dilaudid preferida sobre morfina o fentanilo • No hay predilección por algún AINE • Anestesia epidural en pacientes quienes ameritan altas dosis de opioides por un largo tiempo Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN, Crockett S, et al. American gastroenterological association institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018;154(4):1096–101. http://dx.doi.org/10.1053/j.gastro.2018.01.032
- 27. Pancreatitis Aguda • TRATAMIENTO • EL PAPEL DE LOS ANTIBIÓTICOS EN LA PANCREATITIS AGUDA. • No se recomienda el uso rutinario de antibióticos profilácticos en pacientes con pancreatitis aguda grave. • No se recomienda el uso de antibióticos en pacientes con necrosis estéril • En los pacientes con necrosis infectada, esta indicado el tratamiento antibiótico, tales como carbapenems, quinolonas, y metronidazol. Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN, Crockett S, et al. American gastroenterological association institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018;154(4):1096–101. http://dx.doi.org/10.1053/j.gastro.2018.01.032
- 28. Pancreatitis Aguda • TRATAMIENTO • EL PAPEL DE LA CIRUGÍA EN LA PANCREATITIS AGUDA o En pancreatitis biliar, una colecistectomía se debe realizar antes del alta para evitar una recurrencia. o En pacientes con pancreatitis biliar necrotizante, con el fin de prevenir la infección, la colecistectomía debe aplazarse. o La presencia de pseudoquistes asintomáticos y / o necrosis extrapancreática no justifican la intervención. o En pacientes estables con necrosis infectada, se debe demorar el tratamiento preferiblemente durante más de 4 semanas para permitir licuación de los contenidos y el desarrollo de una pared fibrosa alrededor de la necrosis. o En los pacientes sintomáticos con necrosis infectada, se prefieren los métodos mínimamente invasivos. Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN, Crockett S, et al. American gastroenterological association institute guideline on initial management of acute pancreatitis. Gastroenterology. 2018;154(4):1096–101. http://dx.doi.org/10.1053/j.gastro.2018.01.032
- 30. Pancreatitis Aguda • COMPLICACIONES LOCALES Pancreatitis intersticial edematosa. Pancreatitis necrotizante. Colección aguda peri pancreática. Pseudoquiste pancreático. Necrosis amurallada. Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 31. Pancreatitis Aguda • COMPLICACIONES PERIPANCREÁTICOS Trombosis . Pseudoaneurisma. Síndrome Compartimental abdominal. Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 32. Pancreatitis Aguda • COMPLICACIONES SISTÉMICOS Cardiaco. Pulmonar. Hepático. Renal. Chatila AT, Bilal M, Guturu P. Evaluation and management of acute pancreatitis. World J Clin Cases 2019; 7(9): 1006-
- 33. MUCHAS GRACIAS
Notas del editor
- Disfunción mitocondrial mediada por calcio y muerte celular en pancreatitis aguda. En las células acinares, el alcohol, la colecistoquinina (CCK) y los ácidos biliares provocan la liberación de calcio del retículo endoplásmico (ER) mediada por el receptor de inositol 1,4,5-trifosfato (Ins (1,4,5) P3R). La baja concentración de calcio resultante en el RE desencadena la apertura de la proteína 1 del canal de calcio activada por liberación de calcio (ORAI1), a través de la cual el calcio ingresa a la célula desde el espacio extracelular. Esto da como resultado una elevación patológica global de la concentración de calcio. La elevación del calcio da como resultado la apertura de los poros de transición de la permeabilidad mitocondrial (MPTP) a un estado de alta conductancia, y se produce una pérdida de potencial de membrana a través de la membrana mitocondrial. Este proceso resulta en disfunción mitocondrial y necrosis. La disfunción mitocondrial conduce a la depleción de ATP, lo que altera los mecanismos dependientes de ATP para reducir el calcio citosólico. Este proceso luego acentúa y perpetúa la toxicidad patológica del calcio. La elevación patológica del calcio también causa otras vías citotóxicas, incluida la activación prematura del tripsinógeno, el deterioro de la autofagia y la activación de la vía del factor nuclear κB (NF-κB). La vía NF-κB conduce a la producción de mediadores proinflamatorios. El mecanorreceptor PIEZO1, que contiene propiedades de canal de cationes y se activa por presión, también promueve una mayor entrada de calcio desde el exterior de la célula acinar. CypD, ciclofilina D; PMCA: canal de Ca2 + de la membrana plasmática; SERCA, canal ER liso Ca2 +.
- Activación prematura del tripsinógeno en pancreatitis aguda. En las células acinares, el alcohol y otras toxinas pancreáticas aumentan la síntesis de lisosomas y enzimas digestivas, además de alterar la exocitosis apical de los gránulos de zimógeno en las células acinares al causar disfunción de los microtúbulos. Este proceso da como resultado la acumulación de gránulos de zimógeno. El TNF también puede provocar una activación prematura del tripsinógeno al activar el receptor de TNF (TNFR). Los eventos precedentes culminan en la colocalización en la que los lisosomas y los gránulos de zimógeno se fusionan. La catepsina B activa el tripsinógeno a tripsina una vez que se produce la colocalización. La catepsina B y la tripsina se liberan en el citosol. La catepsina B activa la proteína quinasa que interactúa con el receptor (RIP), que incluye RIP1-RIP3, y la ruta similar al dominio de quinasa de linaje mixto (MLKL), que implica la oligomerización de MLKL. La liberación de proteasa intracitoptosólica también conduce a la activación de la caspasa 3 del verdugo de la apoptosis a través de la liberación del citocromo c (CytC) de las mitocondrias. La fosforilación y oligomerización de MLKL lo trasladan a la membrana celular, provocando la ruptura de la membrana y la necrosis celular.
- Respuesta inmune a la lesión y necrosis de las células acinares en la pancreatitis aguda. Las células acinares lesionadas producen citocinas, quimiocinas y moléculas de adhesión para reclutar células inmunes al sitio de la lesión. Una vez reclutadas, las quimiocinas y citocinas de las células acinares, y los patrones moleculares asociados al daño, activan las células inmunes para amplificar una respuesta inflamatoria. Las vías activadas dentro de los monocitos polarizados en M1 incluyen el factor nuclear κB (NF-κB) y el transductor de señal y activador de la transcripción 3 (STAT3). Los monocitos activan los monocitos en otros órganos, causando lesiones en órganos remotos. Los neutrófilos provocan la activación prematura del tripsinógeno y el estrés oxidativo en las células acinares al liberar sustancias oxidantes. Los neutrófilos también liberan trampas extracelulares de neutrófilos (NET), que causan obstrucción ductal, activación prematura del tripsinógeno e inflamación. Debido a una barrera basolateral rota, que resulta de la lesión de las células acinares por una variedad de toxinas, la grasa intrapancreática está expuesta a la lipasa, que se secreta al intersticio. Las grasas intrapancreáticas y peripancreáticas ricas en triglicéridos son hidrolizadas por la lipasa. Esta reacción libera ácidos grasos libres tóxicos que pueden causar más daño a las células acinares y falla orgánica. CXCL, ligando de quimiocina CXC; HMGB1, proteína 1 de caja de grupo de alta movilidad; ICAM1, molécula de adhesión intercelular 1; MCP1, proteína quimioatrayente de monocitos 1; NFAT, factor nuclear de células T activadas.
- Es importante tener en cuenta que la lipasa y/o amilasa pueden estar elevadas < 3 veces su valor de referencia máximo y esto podría explicarse por las diferencias en la cinética de ambas enzimas, ya que la lipasa comienza a elevarse dentro de las 4-8 horas posteriores al inicio de la PA, presenta un pico a las 24 horas y comienza a descender dentro de los 8-14 días, mientras que la amilasa a menudo aumenta a las 6-24 horas, usualmente presenta un pico a las 48 horas y típicamente tiende a normalizarse durante los siguientes 5-7 días. Además, la determinación de amilasa puede ser normal en pancreatitis causadas por alcohol o por hipertrigliceridemia.
- Es importante tener en cuenta que la lipasa y/o amilasa pueden estar elevadas < 3 veces su valor de referencia máximo y esto podría explicarse por las diferencias en la cinética de ambas enzimas, ya que la lipasa comienza a elevarse dentro de las 4-8 horas posteriores al inicio de la PA, presenta un pico a las 24 horas y comienza a descender dentro de los 8-14 días, mientras que la amilasa a menudo aumenta a las 6-24 horas, usualmente presenta un pico a las 48 horas y típicamente tiende a normalizarse durante los siguientes 5-7 días. Además, la determinación de amilasa puede ser normal en pancreatitis causadas por alcohol o por hipertrigliceridemia.
- Con respecto a las imágenes, en la práctica cotidiana la ecografía es el estudio inicial por imagen más utilizado. La tomografía computada y la resonancia magnética usualmente no son necesarias para establecer el diagnóstico de pancreatitis, y tienen un rol principalmente en los casos donde existe duda diagnóstica.
- Dolor abdominal característico, amilasa y/o lipasa (triacilglicerol acilhidrolasa) plasmáticas > 3 veces su valor de referencia máximo y/o evidencia radiológica de pancreatitis. El dolor característico es epigástrico, de inicio agudo, intenso, persistente y, a menudo, irradiado a dorso, pero en algunos pacientes el dolor puede no ser típico.
- VALIDADA EN 1992 Y EN EL 2000
- PANCREATITIS LEVE no hay falla de órganos, no hay complicaciones sistémicas o locales PANCREATITIS MODERADAMENTE SEVERA Falla de órganos que resuelve en menos de 48 hrs, complicaciones locales y sistémicas PANCREATITIS SEVERA Falla de órganos de manera persistente, falla multiorgánica
- 1. Pancreatitis aguda leve (PAL) se caracteriza por la ausencia tanto de la necrosis (peri) pancreática como de fallo orgánico. 2. Pancreatitis aguda moderada (PAM) se caracteriza por la presencia de cualquier tipo de necrosis (peri) pancreática estéril o fallo orgánico transitorio. 3. Pancreatitis aguda grave (PAG) se caracteriza por la presencia de cualquier grado de necrosis (peri) pancreática infectada o fallo orgánico persistente. 4. Pancreatitis aguda crítica (PAC) se caracteriza por la presencia de necrosis (peri) pancreática infectada y fallo orgánico persistente.
- 200-500 ml por hora, 2500-4000 las primeras 24 horas
- En pacientes con pancreatitis aguda leve que no tienen insuficiencia orgánica o necrosis, no hay necesidad de una resolución completa del dolor o la normalización de los niveles de enzimas pancreáticas antes de iniciar la alimentación oral.39 Una dieta blanda o sólida baja en grasas es segura y se asocia con una hospitalización más corta. permanece que una dieta de líquidos claros con avance lento a alimentos sólidos. La mayoría de los pacientes con pancreatitis aguda leve pueden comenzar con una dieta baja en grasas poco después del ingreso, en ausencia de dolor intenso, náuseas, vómitos e íleo (todos los cuales son inusuales en casos leves de pancreatitis aguda).
- Exacerbaciones de condiciones subyacentes y estos pacientes deben ser ingresados a terapia y en tratamiento multidisciplinario