Este documento resume la historia y conceptos fundamentales de las enzimas. Las enzimas son proteínas que actúan como catalizadores biológicos, acelerando las reacciones químicas sin ser consumidas. Se clasifican según el tipo de reacción que catalizan y su número EC. Su especificidad depende de factores como la orientación, carga eléctrica y distorsión inducida en los sustratos. La cinética enzimática sigue el modelo de Michaelis-Menten.




![Eficiencia enzimática
Se describe con el “turnover number”:
número de moles de sustrato
transformado en producto por mol de
enzima por segundo.
Mayor el “turnover number” mayor la
eficiencia.
Equivale a: Vmax/[Et]
Factores que determinan la
Unidades enzimáticas catálisis (eficiencia)
La concentración de las enzimas se Proximidad y orientación: debe existir una
expresa en términos de su actividad: interacción entre el sustrato y el centro
Unidad enzimática: cantidad de enzima activo.
que produce la transformación de un
micromol de sustrato por minuto bajo Efectos electrostáticos: constante
condiciones definidas. dieléctrica baja lo que permite estabilizar
Actividad específica: número de unidades estados de transición polares; mejor
por miligramo de proteína total. interacción.
Actividad total: número total de unidades
enzimáticas.](https://image.slidesharecdn.com/cap420enzimas-110604161849-phpapp01/85/Cap4-20-enzimas-5-320.jpg)

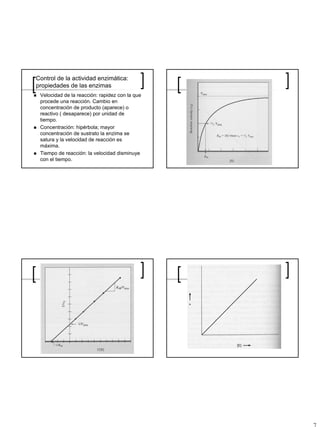




![Control de la actividad enzimática: Control de la actividad enzimática:
cinética de las enzimas cinética de las enzimas
Ecuación Michaelis-Menten Ecuación Michaelis-Menten
KM es igual a la concentración de
V max [S ] sustrato cuando 50% de los centros
activos de la enzima están ocupados.
V =
K M + [S ] También representa cuán fuerte la
enzima se enlaza al sustrato.
VMAX está relacionado con el turnover
V max
Km = [ S ], cuandoVo = number
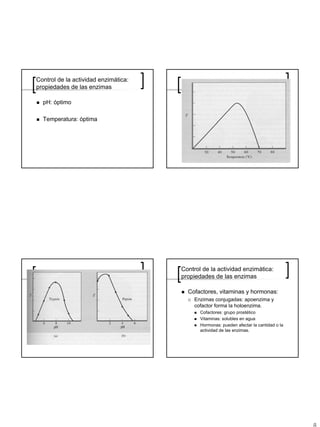
2 Gráfica Lineweaver-Burk
Control de la actividad enzimática:
cinética de las enzimas
Medidas de la actividad enzimática
Ks: mayor la afinidad de la enzima por el
sustrato, mayor la concentración [ES] y
menor el Ks.
Constante de velocidad catalítica:
Vmax/[E], mide la eficiencia de la enzima
cuando la enzima está saturada con
sustrato.
Constante de especificidad: kcat/Km,
ayuda a medir la eficiencia de la enzima.](https://image.slidesharecdn.com/cap420enzimas-110604161849-phpapp01/85/Cap4-20-enzimas-13-320.jpg)



