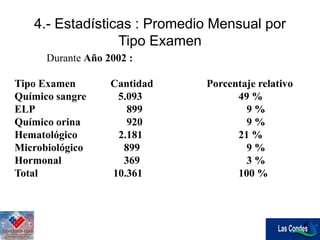
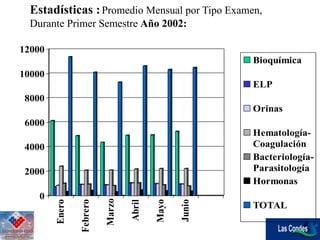
Este documento describe los esfuerzos de un laboratorio clínico para implementar un programa de control de calidad riguroso utilizando controles comerciales de BioRad y reglas estadísticas para monitorear la precisión y exactitud de los análisis. El laboratorio ahora puede cumplir con los estándares internacionales de error y ha reducido la tasa de discordancia clínica del 15% al 3% a través de mejoras en la pre-analítica, analítica y post-analítica.