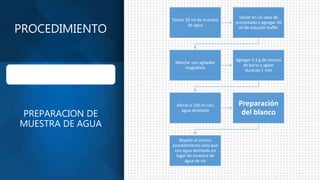
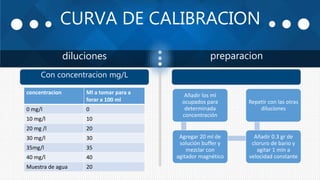
Este documento describe un procedimiento para determinar la concentración de sulfatos en muestras de agua del río Coatzacoalcos utilizando un método turbidimétrico. La muestra se mezcló con una solución amortiguadora y cloruro de bario para formar cristales de sulfato de bario. Se construyó una curva de calibración y la absorbancia de la muestra indicó una concentración de sulfatos de 91.11 mg/L, excediendo el límite máximo de 40 mg/L.









![Calcular la concentración de masa de γ(SO4 2-
) expresada en mg/L de SO4 2-, utilizando la
siguiente ecuación:
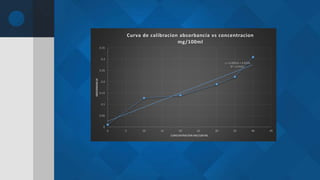
γ(SO4 2-) = [α(λ) - a] / b
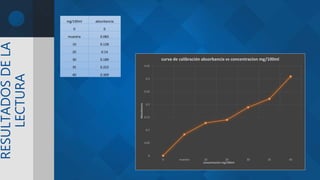
γ(SO4 2-) = [0.083 – 0.0256] / 0.0063
= 9.111 mg/ 100 ml
= 91.11 mg/L
Concentracion de
sulfatos
Donde:
b es la pendiente;
a es la ordenada al origen;
α(λ) es la absorbancia del ion sulfato a la
longitud de onda λ, y
γ(SO4 2-) es la concentración de masa
del ion sulfato expresada en mg/L de
SO4 2-.](https://image.slidesharecdn.com/determinaciondesulfatos-151129082312-lva1-app6891/85/Determinacion-de-sulfatos-14-320.jpg)



