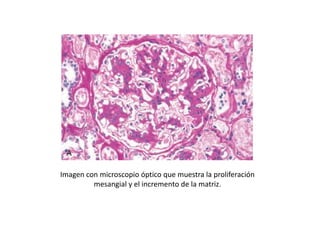
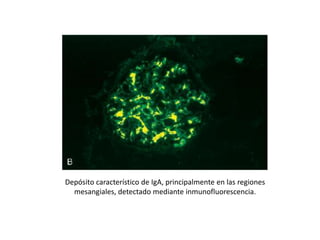
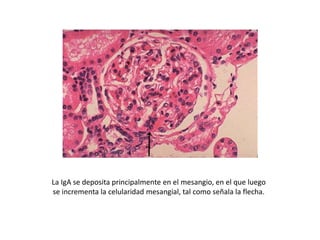
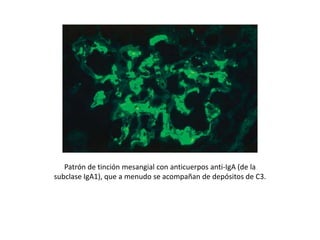
La nefropatía por IgA o enfermedad de Berger se caracteriza por depósitos de inmunoglobulina A en las regiones mesangiales de los riñones. Estos depósitos se producen cuando complejos inmunitarios que contienen IgA se atrapan en el mesangio y activan la vía alternativa del complemento, lo que causa daño renal. Los síntomas incluyen hematuria, a menudo después de una infección, y proteinuria leve. La evolución es variable pero puede progresar lentamente a insuficiencia renal crón