Propiedades termodinámicas de gases
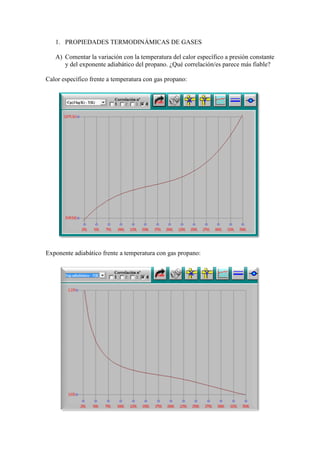
- 1. 1. PROPIEDADES TERMODINÁMICAS DE GASES A) Comentar la variación con la temperatura del calor específico a presión constante y del exponente adiabático del propano. ¿Qué correlación/es parece más fiable? Calor específico frente a temperatura con gas propano: Exponente adiabático frente a temperatura con gas propano:
- 2. -El calor específico del propano en un proceso isobárico se incrementa a medida que la temperatura va aumentado, esto se produce de manera inversa en el exponente adiabático como podemos observar en las gráficas anteriores. Por tanto, podemos decir que ambas correlaciones son fiables. B) Idem aire. Si el rango de trabajo de un equipo que emplea aire a presión atmosférica es 20-150 ºC, ¿es asumible suponer que el aire se comporta como gas perfecto: 1.) Calor específico frente a temperatura con aire: 2.) Exp. Adiabático frente a temperatura con aire:
- 3. -Como podemos observar para el rango de 250-500 K la gráfica 1. se comporta de manera casi lineal, lo cual significa que podemos considerar el aire como un gas ideal (dentro de dicho rango). No obstante, para un rango mayor de temperaturas la relación deja de ser lineal y por tanto, no se comportará como un gas ideal. C) Se desea transportar calor por un conducto evitando que la temperatura del mismo sea demasiado elevada, ¿qué gas (propano o aire) es más adecuado? -La circulación es a presión constante por tanto el calor se asume como: 𝐶 𝑝 = ∆𝑄 ∆𝑇 . Cuando mayor sea Cp menor será la temperatura alcanzada por el fluido. Entre ambos gases, termodinámicamente deberíamos elegir el propano, sin embargo, puede resultar peligroso debido a sus propiedades. D) Se dispone de un compresor de tipo cilindro-émbolo aislado, donde se comprime un gas (inicialmente a presión atmosférica) desde un volumen inicial hasta otro final. ¿Con qué gas (propano o aire) se alcanza mayor presión? -Al tratarse de un ciclo muy rápido el del cilindro, podemos considerarlo adiabático pues los intercambios de calor se consideran despreciables para intervalos de tiempo tan pequeños. Particularizando la relación de las transformaciones politrópicas, para el caso adiabático, obtenemos que: 𝒑 𝟏 ∙ 𝒗 𝟏 𝜸 = 𝒑 𝟐 ∙ 𝒗 𝟐 𝜸 𝒑 𝟐 = 𝒑 𝟏 ∙ ( 𝒗 𝟏 𝜸 𝒗 𝟐 𝜸)
- 4. Como se trata de una compresión podemos asegurar que 𝑝2 > 𝑝1 luego: ( 𝑣1 𝑣2 ) > 1 El gas con mayor gamma en la ecuación de las “adiabáticas” alcanzará una presión mayor, lo que en este caso nos hace decantarnos por el aire. 2. ECUACIONES DE ESTADO A) Representar en el diagrama p-v las isotermas del vapor de agua correspondientes a 550, 600, 650 y 700 K si se asume comportamiento como gas ideal. Isotermas del vapor de agua (550,600,650,700 K):
- 5. B) Idem asumiendo comportamiento como gas de Van der Waals. (presión crítica: 220.9 bar, temperatura crítica: 647.3 K). Isotermas del vapor de agua (gas de Van der Waals): NOTA: Establecer los siguientes límites en los ejes: 0.002-0.03 m3/kg, 0-400 bar C) Si se trabaja con dicha sustancia en condiciones de densidad elevada, ¿es asumible modelar su comportamiento a través de la ecuación de estado del gas ideal? -Altas densidades en un gas implican bajos volúmenes de trabajo, por tanto, como la gráfica nos muestra, en dicha zona de trabajo el comportamiento de las isotermas del vapor de agua está muy lejos de ser ideal o dicho gráficamente, está muy lejos de la linealidad.
- 6. 3. TRANSFORMACIONES TERMODINÁMICAS A) Comparar las siguientes formas de comprimir nitrógeno (inicialmente a 1 bar y 300 K) hasta la décima parte de su volumen: - Adiabática: : Tras compresión Presión = 24.47 bar Temperatura = 734.3 K - Isóbara: Tras compresión Presión = 1 bar T Temperatura = 30 K - Isoterma : Tras compresión Presión = 10 bar Temperatura = 300 K
- 7. - Politrópica n=1.6: Tras compresión Presión = 39.8 bar Temperatura = 1194 K ¿En cuál aumenta más la presión? En la politrópica (n=1.6) ¿Y la temperatura? En la politrópica (n=1.6) ¿En cuál se requiere menos trabajo? En la isobara ¿En cuál disminuye más la entropía? En la isobara. B) Comprobar las respuestas anteriores con diagramas (p-v y T-s) hechos a mano.
- 8. C) Resolver el siguiente ejercicio: Considérese un ciclo termodinámico, al cual se somete una cierta cantidad de aire, compuesto por las siguientes transformaciones: A-B: Expansión isobárica desde A (pA = 1 bar, TA = 365 K) hasta B (TB = 547.5 K). B-C: Caída de presión isócora (pC = 0.48 bar). C-D: Compresión adiabática. D-A: Expansión isoterma. Se pide: - Hallar la variación de energía interna, la variación de entropía y el calor y trabajo intercambiados en cada una de las cuatro transformaciones que componen el ciclo. En la siguiente tabla se resumen los resultados obtenidos con el programa ‘Termo’: A-B B-C C-D D-A V. Energía Interna [KJ/kg] 135.6299 -209.5451 73.9152 0 V. Entropía [KJ/kgK] 0.4178 -0.5384 -0.0001 0.1207 Calor [KJ/kg] 188.2245 -209.545 -0.0013 43.9861 Trabajo [KJ/kg] 52.5947 0.0001 -73.9165 43.9861
- 9. - Representar el ciclo en los diagramas p-V y T-S Diagrama p-V: Diagrama T-S:
- 10. - Hallar la variación total de energía interna y entropía en el ciclo termodinámico, así como el área encerrada por el ciclo en los dos diagramas anteriores.