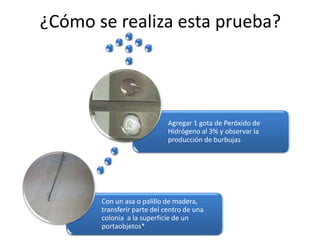
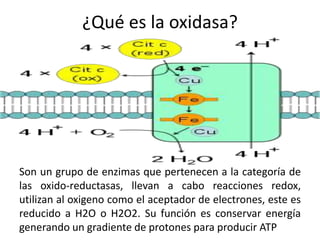
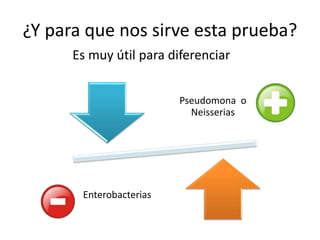
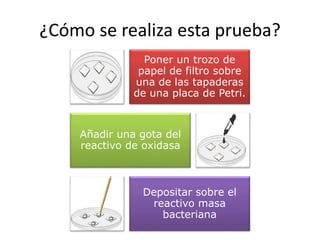
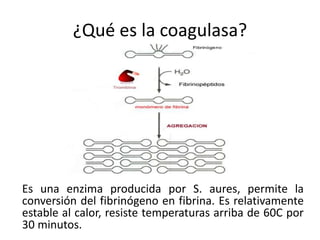
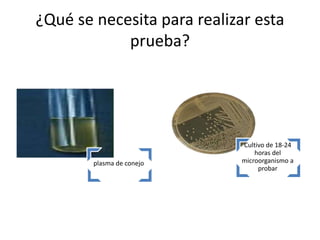
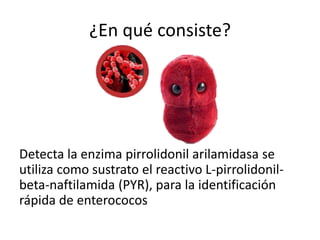
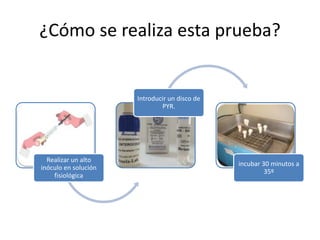
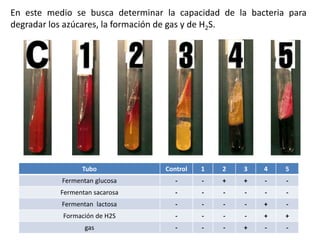
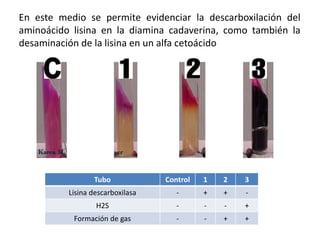
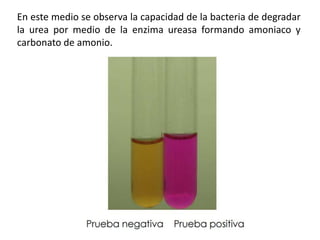
Este documento describe varias pruebas bioquímicas utilizadas para identificar bacterias. Las pruebas incluyen catalasa, oxidasa, coagulasa, PYR, y medios de cultivo diferenciales que detectan la fermentación de azúcares y la producción de enzimas. Estas pruebas permiten diferenciar bacterias basadas en la presencia o ausencia de enzimas específicas.