Pruebas bioquimicas y coprocultivo
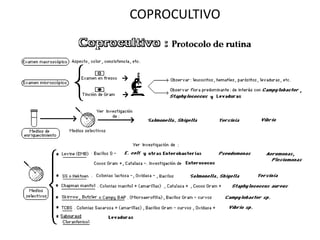
- 1. COPROCULTIVO
- 2. PRUEBAS BIOQUIMICAS Las pruebas bioquímicas son un conjunto de reacciones que determinan la actividad de una vía metabólica de la bacteria a partir de un sustrato que se incorpora en un medio de cultivo y que la bacteria al crecer transforma o no.
- 3. PRUEBAS BIOQUIMICAS CITRATO DE SIMONS FUNDAMENTO: Se utiliza para determinar si un organismo es capaz de utilizar el citrato como única fuente de carbono para el metabolismo en condiciones aeróbicas, provocando alcalinidad. INDICADOR: Azul de Bromotimol. pH INICIAL: 6.9
- 4. INOCULACIÓN: Estría en la superficie. INTERPRETACIÓN: El ensayo es positivo cuando se observa crecimiento a lo largo de la estría, acompañado o no de un viraje de verde a azul por el indicador (pH: 7.6).
- 6. DIFERENCIACIÓN DE GENERO: Salmonella (+), Serratia (+), Klebsiella (+), Edwardsiella (-), Yersinia pseudotuberculosis (-), Yersinia enterocolitica (-). DIFERENCIACIÓN DE ESPECIE: Aeromonas hydrophilia (+), Aeromonas salmonicida ( - ), Bordetella pertussis ( - ), otras Bordetella (+), Moraxella osloensis (+), Pseudomonas cepacia (+), Pseudomonas maltophilia(-).
- 7. AGAR HIERRO DE KLIGLER (AHK) y TSI Ó AHTA (AGAR HIERRO TRIPLE AZUCAR) FUNDAMENTO: Determinar la capacidad de un organismo de atacar el hidrato de carbono especifico incorporado en un medio de crecimiento básico, con producción o no de gases, con la determinación posible de H2S (ác. sulfhídrico).
- 8. El agar se prepara en forma de pico de flauta. Esto determina que existan 2 cámaras de reacción dentro del mismo tubo. La porción inclinada (pico) expuesta en toda su superficie al oxígeno es aerobia y la porción inferior (fondo) está protegida del aire y es relativamente anaerobia. La porción inclinada del tubo que está expuesta al oxígeno atmosférico tiende a tornarse alcalina (roja por el rojo fenol) por la utilización aerobia de las peptonas.
- 9. En el fondo del tubo, donde no hay oxígeno, la degradación proteica es mínima y se pueden detectar pequeñas cantidades de ácido por la aparición de un color amarillo (indicador: rojo fenol). En ausencia de fermentación de carbohidratos, no se formarán ácidos y por la producción de aminas en el pico, todo el medio quedará rojo. Esto se da en organismos no fermentadores. INDICADOR: Para ambos rojo de fenol. pH INICIAL: 7.3 INOCULACIÓN: Por picadura y estría.
- 10. PROCEDIMIENTO: utilizaremos tubos inclinados de agar "Kligler-Iron". Sembramos con la bacteria problema comenzando por realizar una picadura desde el centro del "slant" hasta el fondo del tubo y al retroceder realizamos una estría en la superficie del agar inclinado. Se lleva a incubar a 37oC durante 24 horas.
- 11. Si transcurrido este tiempo aparece coloración amarilla en el pico de flauta, la lactosa que contiene el medio ha sido utilizada aerobiamente, produciendo suficiente acidez como para virar el medio de cultivo; si aparece esta coloración en el fondo, ha habido fermentación de la glucosa y si además observamos que en el fondo del tubo se ha roto el agar, podemos decir que ha habido producción de gas en la fermentación de la glucosa.
- 12. KLIGLER
- 13. A/A/G A/K K/H2S MEDIO SIN INOCULAR MEDIO TSI
- 14. A/A/G o SIN GAS. En medio TSI Escherichia. Klebsiella. Enterobacter. Serratia. A/A/H2S TSI Arizona. Citrobacter. Proteus mirabilis. Proteus bulgaris. A/A TSI Yersinia enterocolitica. K/A. TSI Yersinia pestis. K/A TSI Yersinia pseudotuberculosis K/A/G/ H2S. Kligler y TSI Edwarsiella. Arizona. Citrobacter. Salmonella typhi, S. enteritidis; S. cholera-suis. Proteus mirabilis y vulgaris.
- 15. FERMENTACIÓN DE CARBOHIDRATOS (VP Y RM) VOGES - PROSKAUER (Producción de Acetoína) FUNDAMENTO VP: Uno de los test del IMViC ( Indol, Rojo de Metilo, Voges Proskauer, Citrato) para enterobacterias es el Voges Proskauer. Las especies que llevan a cabo la fermentación a butanodiol de la glucosa acumulan acetoína (acetilmetilcarbinol) en el medio. Las bacterias se inoculan en caldo glucosa-peptona.
- 16. Las especies que llevan a cabo la fermentación butanodiólica de la glucosa forman acetoína en el medio. Se añade alfanaftol y hidroxido de potasio en medio alcalino. La acetoína se convierte en diacetilo con la aparición de un color rojo.
- 17. INDICADOR: NINGUNO. pH INICIAL: Ajustar a 6.9 PROCEDIMIENTO: Inocular el caldo VP con un cultivo puro de no más de 24 horas del microorganismo en estudio. Incubar a 37°C durante 24 horas. Luego de finalizado el tiempo de incubación transferir 1 ml del caldo VP a un tubo limpio y agregar 0,6 ml (6 gotas)de alfa-naftol al 5% y 0,2 ml (2 gotas) de KOH al 40%. Agitar el tubo cuidadosamente para exponer el medio al oxígeno atmosférico y dejarlo reposar durante 20 a 30 minutos.
- 18. POSITIVO pH 4.2 NEGATIVO pH 6.0 •INTERPRETACIÓN: prueba positiva se da por aparición de un color rojo en el tubo (acetilmetilcarbinol). pH: 4.2, negativa sin cambio de color pH:6.0., sin inocular pH 6.9.
- 19. DIFERENCIACIÓN DE GENERO: Klebsiella pneumoniae (+), Enterobacter (+), Escherichia coli (-) DIFERENCIACIÓN DE ESPECIE: Klebsiella pneumoniae (+), K. ozaenae (-), K. rhinoscheromatis (-), Enterobacter hafniae 25 ºC (+), a 37ºC generalmente (+), Yersinia enterocolitica a 25ºC (+), a 37 ºC (-).
- 20. FUNDAMENTO PARA RM. Comprobar la capacidad de un organismo de producir y mantener estables los productos terminales de la fermentación de la glucosa que son ácidos, como ác. fórmico, ác. acético, ác. láctico, y ác. succínico. Para vencer la capacidad amortiguadora del sistema. INDICADOR: NINGUNO. pH INICIAL: 6.9 PROCEDIMIENTO: Inocular el caldo RM con un cultivo puro de no más de 24 horas del microorganismo en estudio. Incubar a 37°C durante 24 horas. Añadir al tubo 5 gotas del reactivo rojo de metilo sin agitar. RM
- 21. POSITIVO NEGATIVO •INTERPRETACIÓN: La presencia de un anillo rojo en la parte superior del tubo es una prueba positiva, si no se forma es negativa.
- 22. DIFERENCIACIÓN DE GENERO: Escherichia coli. (+), Enterobacter aerogenes (-), Enterobacter cloacae, (-), Klebsiella por lo general (-). DIFERENCIACIÓN DE ESPECIE: Yersinia (+), no entéricos Gram negativos (-). Listeria monocytogenes (-)
- 23. METABOLISMO DE AMINOACIDOS LIA (AGAR DE HIERRO Y LISINA) (Lysine Iron Agar) FUNDAMENTO: Permite diferenciar los microorganismos que producen descarboxilación o desaminación de la lisina, se puede detectar además H2S, y es más sensible que el TSI para la detección de H2S, por la reacción de H2S con la sal pesada, citrato férrico de amonio para darnos un precipitado negro.
- 24. PROCEDIMIENTO: Inocular por picadura y estría, en un tubo con medio LIA incubar los tubos a 37ºC durante 24 Hrs. INDICADOR: Púrpura de Bromocresol pH INICIAL: 6,7 +/- 0,2
- 25. INTERPRETACIÓN: Sin inocular: Color violeta – Descarboxilación positiva: color púrpura en el fondo. – Descarboxilación negativa: color amarillo en el fondo. – Desaminación positiva: color rojo naranja en la superficie del medio. – Desaminación negativa: sin cambio en el color en la superficie. – Producción H2S: presencia de precipitado negro.
- 26. 1. Descarboxilación de la lisina negativo. 2. Descarboxilación positiva, con gas y H2S. 3. Descarboxilación negativa, pero desaminación positiva, con utilización de Glucosa en el fondo y gas
- 27. OTRAS PRUEBAS MIO (MOVILIDAD, INDOL y ORNITINA) FUNDAMENTO: Pone de manifiesto la presencia de enzimas ornitina descarboxilasa y triptofanasa, además el medio es semisólido, permitiendo evidenciar así la movilidad entre el medio a las bacterias con flagelos. También permite observar la presencia de indol que es el producto metabolico del aminoácido triptofano
- 28. En el caso de la ornitina es descarboxilada por una enzima ornitina descarboxilasa dando como producto final la putrescina, durante la descarboxilación el pH aumenta. INDICADOR: Púrpura de bromocresol pH INICIAL: 6.0 color púrpura intenso brillante. PROCEDIMIENTO: Inocular por picadura.
- 29. INTERPRETACIÓN. MOVILIDAD. En el caso de la movilidad, se observa en todo el medio crecimiento. INDOL. Para visualizar la presencia de indol, agregar 5 gotas de Kovacs o 5 gotas de Erlinch, este con 5 mL de cloroformo. Indol positivo se observa un anillo rojo en la superficie (no agitar). ORNITINA La descarboxilación provoca una desviación del pH hacia la alcalinidad dando un color más intenso, lo que indica que es positiva, en caso de ser una prueba negativa el medio se vuelve amarillo.
- 30. MIO La reacción positiva a la ornitina está dada por un color púrpura del medio. Debido a la fermentación de la glucosa se reduce el pH produciendo una condición ácida y originando que el indicador de pH púrpura de bromocresol vire al amarillo. MOVILIDAD (+) ORNITINA (-) MEDIO SIN INOCULAR
- 31. MIO El indol, es producido a partir del triptofano por los microorganismos que contienen la enzima triptofanasa. El desarrollo de un color rojo luego de agregar unas gotas de reactivo de Kovac´s o de Erlich, indica un resultado positivo.
- 32. INTERPRETACION DEL MEDIO MIO Movilidad: -Resultado positivo: presencia de turbidez o crecimiento mas allá de la línea de siembra. -Resultado negativo: crecimiento solamente en la línea de siembra. 2-Ornitina decarboxilasa: -Resultado positivo: color púrpura. -Resultado negativo: color amarillo. A veces se puede desarrollar un color violáceo en la superficie del medio. 3-Prueba del indol: La prueba de indol se realiza una vez que se ha determinado la movilidad y la prueba de ornitina. -Resultado positivo: color rojo al agregar el reactivo revelador. -Resultado negativo: el color del reactivo revelador permanece incoloro- amarillento.
- 33. DIFERENCIACIÓN DE GENERO: Edwarsiella ( + ), Salmonella ( - ), Escherichia coli (por lo general +), de Klebsiella-Enterobacter (por lo general -) DIFERENCIACIÓN DE ESPECIE: Bacillus alvei ( + ), otras especies de Bacillus ( - ), Haemophilus influenzae y Haemophilus haemoglobinophilus (+), de otras que son ( - ), Pasteurella multocida y Pasteurella pneumotropica ( + ), de la Pasteurella haemolytica, y Pasteurella ureae ( - ), Proteus mirabilis ( - ), de otras especies ( + ).
- 34. SIM (MOVILIDAD, INDOL y SULFURO) FUNDAMENTO: MOVILIDAD. Sirve para ver la movilidad de ciertas bacterias con flagelos, esto a que el agar es semisólido. Las cepas móviles pueden apreciarse en este medio, por la turbidez que producen alrededor de la punción de siembra. INDOL. Permite evidenciar la producción de Indol que es el producto metabólico del aminoácido triptofano.
- 35. PRUEBA DE ÁCIDO SULFHÍDRICO. Determinar si se libera ácido sulfhídrico (H2S), por acción enzimática de los aminoácidos que contienen azufre, como la peptona, cisteína, la cistina y el tiosulfato, todos son fuente de azufre produciendo una reacción visible de color negro, la enzima responsable es la cisteinasa. por la reacción de H2S con la sal pesada, citrato férrico de amonio para darnos un precipitado negro.
- 36. INDICADOR. Ninguno. Medio preparado color ámbar. pH INICIAL. pH final: 7.3 ± 0.2 PROCEDIMIENTO. Inoculación por picadura.
- 37. FENILALANINA FUNDAMENTO. Determina la capacidad de la bacteria para desaminar el aminoácido fenilalanina en ácido fenil pirúvico por acción de la enzima Fenilalanina desaminasa, esto va a producir una acidificación del medio. pH INICIAL: 7.3 ± 0.2 INOCULACIÓN: Estría en la superficie.
- 38. Reactivo: agregar 4-5 gotas de cloruro férrico al 10% Reacción positiva: Aparece una coloración verde- azulada en la superficie después de 1- 5 minutos.
- 39. Positivo: Especies de Proteus, Moraxella phenylpyrouvica. Negativo: otro tipo de Moraxella.
- 40. UREASA FUNDAMENTO: Determinar la capacidad de un microorganismo de desdoblar la urea, formando dos moléculas de amoníaco por la acción de la enzima ureasa. Esta actividad es característica de todas las especies de Proteus y da positivo también para Klebsiella Positivo: Bordetella parapertussis. Bordetella bronchispetica, Moraxellla phenylpyrouvica, Pasteurella pneumotropica. Negativo: Bordetella pertussis, Escherichia coli, Yersenia pestis,
- 41. pH inicial: 6.8 Ácido: Color amarillo. pH 6.8 Alcalino: Color rojo a rosado pH 8.4 Medio no inoculado: Color amarillo naranja pH 6.8 INDICADOR: Rojo de fenol. INOCULACIÓN: Asada
- 42. Incubar a 35 °C Observar la reacción en 8, 12, 24 y 48 de incubación.