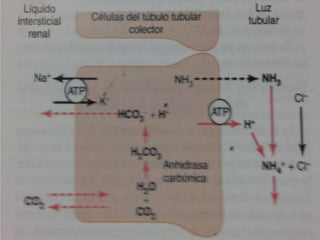
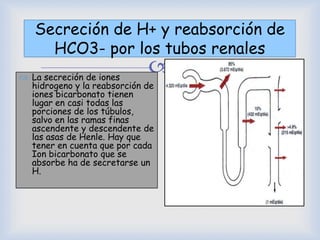
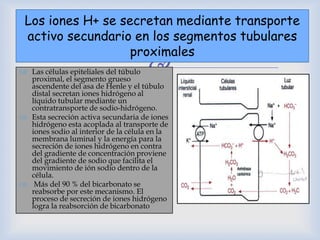
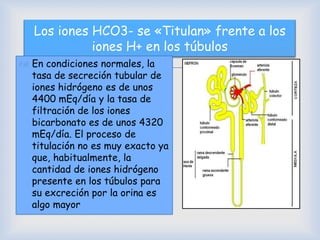
El documento detalla la regulación del pH en fluidos corporales, explicando que esta regulación es crítica para la actividad biológica y es mantenida por sistemas como los pulmones y los riñones. Describe cómo el equilibrio ácido-base se controla a través de la eliminación de CO2 y la excreción de H+ y HCO3- por los riñones, así como el uso de amortiguadores como bicarbonato y fosfato. Además, se menciona la importancia del sistema respiratorio en la regulación del pH y cómo las condiciones como la acidosis y alcalosis son manejadas por el cuerpo.


![Concentraciones de iones H y pH
I. pH=log 1/[H+] = -log[H+]
• Ph: -log[H+]
pH:-log[0.00000004]
pH:7.4
De la formula de pH puede verse que el pH y la
[H+] son inversamente proporcional.
↑Ph = ↓[H+]
↓Ph = ↑ [H+]
SANGRE
Iones de hidrogeno
en la sangre.
(40nEq/l)](https://image.slidesharecdn.com/regulacionacidobsica-131001221808-phpapp02/85/Regulacion-Acido-Basica-4-320.jpg)


![2.El centro respiratorio:
Regula la eliminación de CO2(y por tanto de H2CO3) del
liquido extracelular.
3.Los riñones:
Papel fundamental para el equilibrio de [H+] , que
pueden excretar una orina ya sea acido o básica lo que
permite normalizar la [H+ ] en el liq. Extracelular.
Defensas frente a los cambios en la concentración de
H+:amortiguadores, pulmones y riñones.](https://image.slidesharecdn.com/regulacionacidobsica-131001221808-phpapp02/85/Regulacion-Acido-Basica-7-320.jpg)
![1.
AMORTIGUADORES,BUFFER O
TAMPONES
Los sistemas encargados de evitar grandes variaciones
del valor del pH son los denominado “amortiguadores”
El limite inferior del pH con el que la vida es posible unas
cuantas horas es de alrededor de 6.8 y el limite superior de
alrededor de 8.
Un ejemplo extremo de un liquido orgánico acido es el HCl
secretado por las células oxinticas de la mucosa del
estomago. La [H+] en estas células es unos 4 millones de
veces mayor que en la sangre, con un pH de 0.8](https://image.slidesharecdn.com/regulacionacidobsica-131001221808-phpapp02/85/Regulacion-Acido-Basica-8-320.jpg)







![
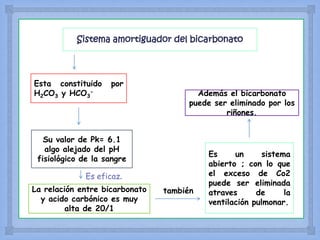
Es la 2da línea de defensa frente a los trastornos del
equilibrio ácido – básica.
Ventilación
elimina
CO2
[H+]
Ventilación
Aumenta
CO2
[H+]](https://image.slidesharecdn.com/regulacionacidobsica-131001221808-phpapp02/85/Regulacion-Acido-Basica-18-320.jpg)


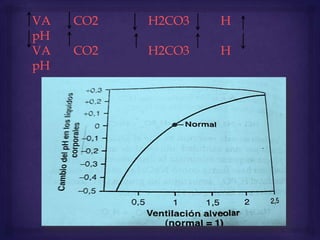
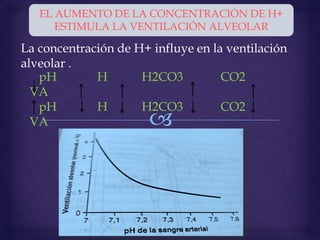
![El aumento de [H+] estimula la respiración y el aumento de la ventilación
alveolar reduce la concentración de H+ , que tendrá que volver a su valor
normal. Esto es siempre que se produzca un aumento superior al valor
normal de la concentración [H+]
Por el contrario , si [H+] se reduce por debajo de los límites normales, la
ventilación alveolar disminuirá , con lo que la concentración de H+
volverá a elevarse y alcanzar la normalidad.
CONTROL POR RETROALIMENTACIÓN DE LA
CONCENTRACIÓN DE H+ A TRAVÉS DEL
SISTEMA RESPIRATORIO](https://image.slidesharecdn.com/regulacionacidobsica-131001221808-phpapp02/85/Regulacion-Acido-Basica-23-320.jpg)




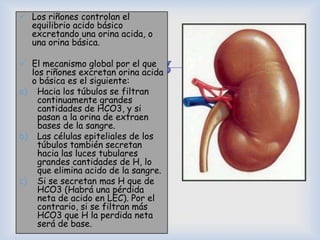
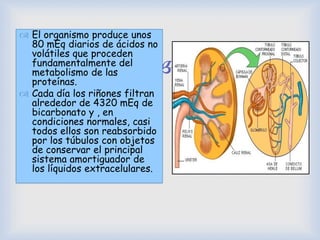


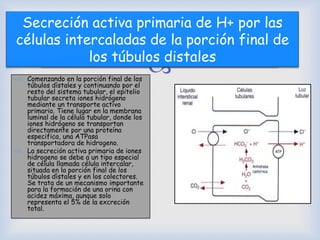



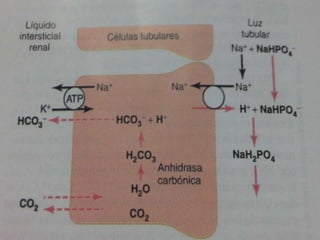


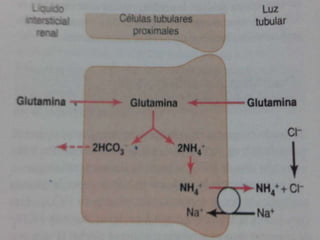
![ El sistema amortiguador de amoniaco-amonio está sujeto
a un control fisiológico.
[H+ ] estimula Metabolismo renal de la glutamina
formación de NH4
+ y HCO3
-
[H+ ]
La cantidad de H+ eliminados por el sistema
amortiguador de amoniaco representa alrededor del 50%
del ácido excretado y el 50% de HCO3
- nuevo generado
por los riñones.
En la acidosis crónica , la excreción de NH4
+
aumenta mucho , pudiendo alcanzar cifras de incluso
500mEq/día
La acidosis crónica aumenta
la excreción de NH4
+](https://image.slidesharecdn.com/regulacionacidobsica-131001221808-phpapp02/85/Regulacion-Acido-Basica-43-320.jpg)