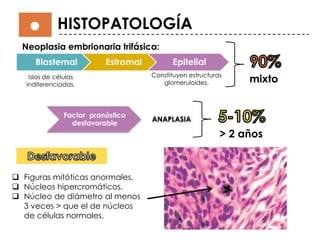
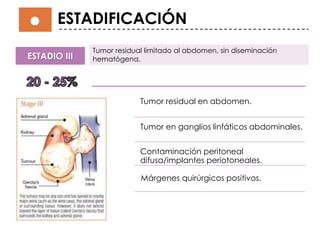
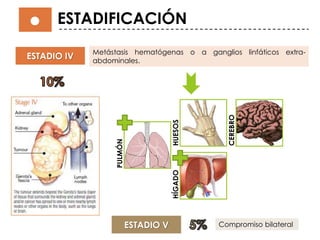
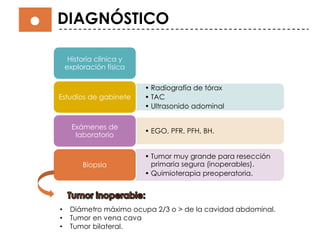
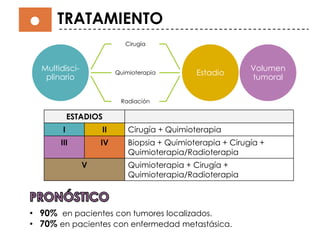
Este documento describe el tumor de Wilms o nefroblastoma, un tumor embrionario maligno del riñón que afecta principalmente a niños menores de 5 años. Se presenta de forma esporádica en el 99% de los casos y su tratamiento implica cirugía, quimioterapia y en algunos casos radioterapia, dependiendo del estadio y características del tumor.