Ejercicios de vamos a repasar quimica
•
0 recomendaciones•9 vistas
Ejercicios de vamos a repasar
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Evaluación estequiometría química primer año medio

Evaluación estequiometría química primer año medio
Ejercicios Estequiometria solución ácido-base (psu 2003-2011)

Ejercicios Estequiometria solución ácido-base (psu 2003-2011)
Similar a Ejercicios de vamos a repasar quimica
Similar a Ejercicios de vamos a repasar quimica (20)
Último
Último (20)
DISEÑO DE ESTRATEGIAS EN MOMENTOS DE INCERTIDUMBRE.pdf

DISEÑO DE ESTRATEGIAS EN MOMENTOS DE INCERTIDUMBRE.pdf
cuadernillo_cuentos_de_los_valores_elprofe20 (1).docx

cuadernillo_cuentos_de_los_valores_elprofe20 (1).docx
Pasos para enviar una tarea en SIANET - sólo estudiantes.pdf

Pasos para enviar una tarea en SIANET - sólo estudiantes.pdf
Lecciones 07 Esc. Sabática. Motivados por la esperanza

Lecciones 07 Esc. Sabática. Motivados por la esperanza
Bitacora de Inteligencia Artificial y Herramientas Digitales HD4 Ccesa007.pdf

Bitacora de Inteligencia Artificial y Herramientas Digitales HD4 Ccesa007.pdf
Diapositivas unidad de trabajo 7 sobre Coloración temporal y semipermanente

Diapositivas unidad de trabajo 7 sobre Coloración temporal y semipermanente
Diseño Universal de Aprendizaje en Nuevos Escenarios JS2 Ccesa007.pdf

Diseño Universal de Aprendizaje en Nuevos Escenarios JS2 Ccesa007.pdf
PLAN LECTOR QUINTO 2023 educación primaria de menores Quinto grado

PLAN LECTOR QUINTO 2023 educación primaria de menores Quinto grado
Escucha tu Cerebro en Nuevos Escenarios PE3 Ccesa007.pdf

Escucha tu Cerebro en Nuevos Escenarios PE3 Ccesa007.pdf
El liderazgo en la empresa sostenible, introducción, definición y ejemplo.

El liderazgo en la empresa sostenible, introducción, definición y ejemplo.
Época colonial: vestimenta, costumbres y juegos de la época

Época colonial: vestimenta, costumbres y juegos de la época
novelas-cortas--3.pdf Analisis introspectivo y retrospectivo, sintesis

novelas-cortas--3.pdf Analisis introspectivo y retrospectivo, sintesis
ACERTIJO CÁLCULOS MATEMÁGICOS EN LA CARRERA OLÍMPICA. Por JAVIER SOLIS NOYOLA

ACERTIJO CÁLCULOS MATEMÁGICOS EN LA CARRERA OLÍMPICA. Por JAVIER SOLIS NOYOLA
Lineamientos de la Escuela de la Confianza SJA Ccesa.pptx

Lineamientos de la Escuela de la Confianza SJA Ccesa.pptx
MINEDU BASES JUEGOS ESCOLARES DEPORTIVOS PARADEPORTIVOS 2024.docx

MINEDU BASES JUEGOS ESCOLARES DEPORTIVOS PARADEPORTIVOS 2024.docx
Ejercicios de vamos a repasar quimica
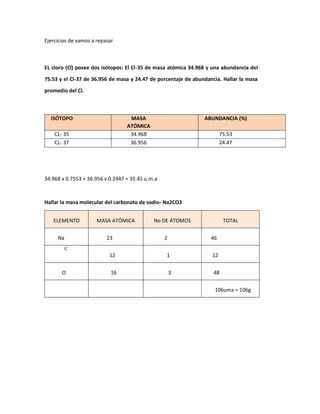
- 1. Ejercicios de vamos a repasar EL cloro (Cl) posee dos isótopos: El Cl-35 de masa atómica 34.968 y una abundancia del 75.53 y el Cl-37 de 36.956 de masa y 24.47 de porcentaje de abundancia. Hallar la masa promedio del Cl. ISÓTOPO MASA ATÓMICA ABUNDANCIA (%) CL- 35 34.968 75.53 CL- 37 36.956 24.47 34.968 x 0.7553 + 36.956 x 0.2447 = 35.45 u.m.a Hallar la masa molecular del carbonato de sodio- Na2CO3 ELEMENTO MASA ATÓMICA No DE ÁTOMOS TOTAL Na 23 2 46 C 12 1 12 O 16 3 48 106uma = 106g
- 2. Calcular el número de moles y de moléculas que hay en 85 g de NaCl X moles de NaCl = 85g de NaCl x 1 mol de NaCl / 58,5g de NaCl = 1,45 moles de NaCl X moléculas de NaCl = 1,45 moles de NaCl x 6.022 moléculas de NaCl / 1 mol NaCl= 6022 10°24 . Clasifique las siguientes reacciones según criterios anteriores a) H2SO4 + NaOH ---------- Na2SO4 + 2 H2O Síntesis b) ZnO ------------- 2 Zn + O2 Descomposición c) 2 MgO + H2O ----------- Mg(OH)2 Composición d) 2 C + H2 ----------- C2 H2 + E Exotérmicas e) Fe + CuSO4 ----------- FeSO4 + Cu Sustitución 2. Complete las siguientes ecuaciones teniendo en cuenta su clasificación a) 2 KClO3 ------------ kcl + O2 b) 2 HCl + Ca(OH)--------- cacl2 + h2o c) Zn + HBr --------- znbr + h d) Na2S + MgSO4 --------- Balancear las siguientes ecuaciones por el método de inspección simple a) Fe(OH)3 ----------- Fe2O3 + H2O Fe2O3 + 3H2O → 2Fe(OH)3 b) C3H8 + O2 -------- CO2 + H2O C3H8 + 5O2 → 3CO2 + 4H2O 2. Balancear las siguientes ecuaciones por el método algebraico a) Na2O + H2O ---------- NaOH Na2O + H2O → 2NaOH b) AgNO3 + CuCl2 ---------- AgCl + Cu(NO)3 2AgNO3 + CuCl2 → Cu(NO3)2