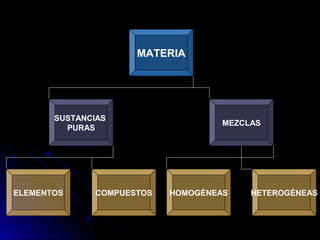
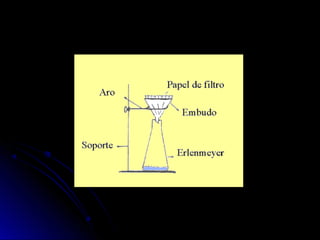
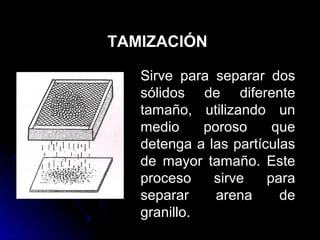
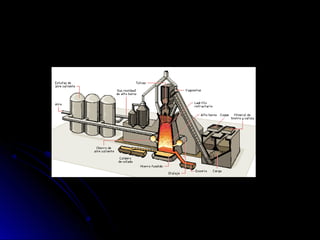
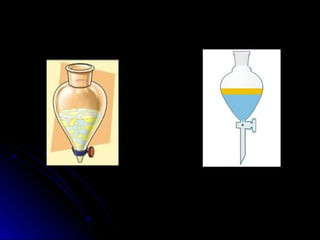
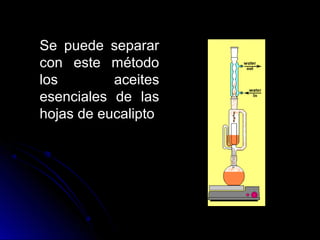
Este documento describe los diferentes tipos de sustancias y mezclas, así como los métodos para separar mezclas. Las sustancias se dividen en puras (elementos y compuestos) y mezclas (homogéneas y heterogéneas). Las mezclas se pueden separar usando procesos mecánicos, físicos, de disolución o químicos como la precipitación.