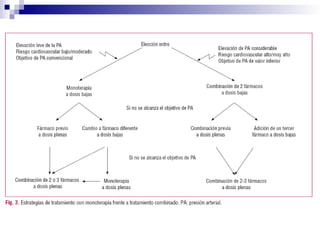
Este documento presenta las guías europeas de 2007 para el tratamiento de la hipertensión arterial. Resume la clasificación del riesgo cardiovascular y las variables clínicas utilizadas para estratificar el riesgo. También describe los métodos de diagnóstico de la hipertensión y la detección de lesiones de órgano diana, así como las evidencias del tratamiento y los objetivos terapéuticos.