Entalpía, Entropía, Energía Libre
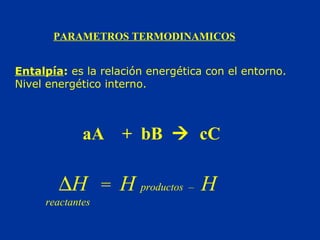
- 1. Entalpía: es la relación energética con el entorno. Nivel energético interno. PARAMETROS TERMODINAMICOS aA + bB cC ∆H = H productos – H reactantes
- 3. POR EJ: H2O (s) H2O (l) CH4 (g) + 2O2 (g) CO2 (g) + 2H2O (l) PROCESO INVERSO.....CAMBIA EL SIGNO (∆H = 6,01 kj) (∆H = – 890, 4 kj)
- 4. EJERCICIO: SEGÚN LA ECUACION TERMOQUIMICA: 2 SO2 (g) + O2 2 SO3 (g) CALCULE EL CALOR LIBERADO CUANDO 74,6 g DE SO2 SE CONVIERTEN EN SO3 (∆H = – 99 kj)
- 5. ¿ COMO CALCULAR LA ENTALPIA DE UNA REACCION? ... CONOCER EL ∆H DE FORMACIÓN DE LAS SUSTANCIA EJEMPLO: DETERMINAR LA ENTALPIA DE REACCION DE FORMACION DEL CO2 C (grafito) + O2 (g) CO2 (g) (∆Hº f = – 393,5 kj/mol)
- 6. EJEMPLO: FORMACION DEL METANO C (grafito) + 2 H2 (g) CH4 a) C (grafito) + O2 (g) CO2 (g) b) 2H2 (g) + O2 (g) 2H2O (l) c) CH4 (g) + 2O2 (g) CO2 (g) + 2H2O LEY DE HESS:LEY DE HESS: “ Cuando un reactivo se convierte en producto, el cambio de entalpía es el mismo independientemente de si se efectúa en un paso o en una serie de pasos” (∆H = – 393,5 kj) (∆H = – 571,6 kj) (∆H = – 890, 4 kj)
- 7. CALCULE LA ENTALPIA DE FORMACION DEL ACETILENO (C2H2) 2 C (grafito) + H2 (g) C2H2 (g) a) C (grafito) + O2 (g) CO2 (g) b) H2 (g) + ½ O2 (g) H2O (l) c) 2C2H2 (g) + 5O2 (g) 4CO2 (g) + 2H2O (l) (∆H = – 393,5 kj) (∆H = – 285,8 kj) (∆H = – 2598,8 kj)
- 8. Graficando dichos procesos seríaGraficando dichos procesos sería Proceso EXOTERMICO Proceso ENDOTERMICOProceso EXOTERMICO Proceso ENDOTERMICO (libera energía) (absorbe energía)(libera energía) (absorbe energía)
- 9. TERMODINAMICA ES PREDECIR SI UNA REACCION ES O NO ESPONTANEA PROCESOS ESPONTANEOS DISMINUYEN LA ENERGIA DEL SISTEMA EL CARÁCTER EXOTERMICO FAVORECE LA ESPONTANEIDAD PERO NO LA GARANTIZA
- 10. Entropía: es la organización del sistema, grado de orden o desorden de la materia. (∆S) Cuando una reacción tiende al orden (∆S < 0) si la reacción tiende al desorden (∆S > 0) S sólido < S líquido << S gas
- 11. EJERCICIO: PREDIGA SI EL CAMBIO DE ENTROPIA ES > O < a)CONGELAMIENTO DE ETANOL b) EVAPORACIO DE BROMO LIQUIDO EN UN RECIPIENTE A TEMPERATURA AMBIENTE c) DISOLUCION DE SACAROSA EN AGUA d) ENFRIAMIENTO DE NITROGENO GASEOSO
- 12. LA ENTROPIA DEL UNIVERSO AUMENTA EN UN PROCESO ESPONTANEO Y SE MANTIENE CONSTANTE... (∆S universo = ∆S sistema + ∆S entorno)
- 13. Para el proceso espontáneo: Para un sistema en equilibrio, la entropía es cero: Cuando hay menor entropía o se tiende al orden, tenemos: (∆S universo = ∆S sistema + ∆S entorno) > 0 Por lo tanto ∆S (+) (∆S universo = ∆S sistema + ∆S entorno) = 0 (∆S universo = ∆S sistema + ∆S entorno) < 0 Por lo tanto ∆S (–)
- 14. Graficando dichos procesos sería
- 15. Energía Libre de Gibbs: Parámetro que indica o predice la dirección de cualquier cambio espontáneo en un sistema a T y P constante. Por lo tanto: - Si ∆G < 0 , el proceso es ESPONTANEO, la reacción ocurrirá. - Si ∆G = 0 , el sistema está en EQUILIBRIO, sin cambio. - Si ∆G > 0 , el proceso NO es ESPONTANEO, la reacción no ocurrirá. (∆G = ∆H sistema – T∆S entorno)
- 16. Termodinamica MateriaMateria Estudia Reacciones Químicas Representadas por Sus parametros de medición son Entalpía Entropía Energía Libre Exotermico ∆H (-) Endotermico ∆H (+) Indica Orden ∆S (-) Desorden ∆S (+) Indica Espontaneo ∆G (-) No Espontaneo ∆G (+) Indica ENERGIA
