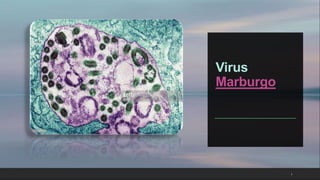
Virusadaaaaaaaaa
- 2. Indice: 1. Casos documentado 2. Anatomia patológica 3. Modalidades de contagio 4. Diagnostico 5. Terapia 6. resumen 2
- 3. Primeros casos documenados 1. El 8 de enero de 1980, enfermó en Kenia, Charles Monet, un francés de 56 años que, a pesar de los cuidados, falleció siete días más tarde. Monet presentó fiebre repentina, seguida de cefalea, diarrea y vómitos. Se cree que Monet se contagió al visitar la cueva Kitum, en el Monte Elgon, frecuentada por numerosas especies de animales que podrían ser reservorios del virus. El médico que había tratado de reanimar a Monet enfermó 9 días después, logrando sobrevivir. 2. El 13 de agosto de 1987, fue hospitalizado, asimismo en Kenia, un muchacho danés de 15 años con un cuadro de cefalea, malestar general, fiebre y vómitos, de tres días de duración. A pesar de la intensa terapia de apoyo, murió al undécimo día de enfermedad. También había visitado la cueva de Kitum. 3. Entre 1998 y 2000 hubo una epidemia en la República Democrática del Congo, con 154 personas enfermas de las que murieron 128 (mortalidad del 83 %). La mayor parte de los casos ocurrió entre obreros de la mina de oro de Durba, en el noroeste del país, y luego en la aldea vecina de Watsa. La transmisión secundaria fue escasa, aunque se contagiaron algunos familiares que habían participado directamente en el cuidado de los pacientes. Análisis virológicos que se realizaron a continuación indicaron que se habían introducido cepas virales de diversos tipos, pero no se identificó la fuente. 3
- 4. Anatomía patológica Es común la presencia de necrosis focales de hígado, nódulos linfáticos, testículos, ovarios, pulmones, riñones y órganos linfoides. En el hígado se localizan cuerpos eosinófilos (similares a los cuerpos de Councilman) y en el pulmón se notan indicios de pulmonitis intersticial y de endoarteritis de las arterias pequeñas. La necrosis focal de los órganos linfoides es bastante característica, mientras que la necrosis tubular renal ocurre sobre todo en las últimas fases de enfermedad. En el sistema nervioso hay infartos hemorrágicos múltiples y proliferación de las células de la glía. En los vasos sanguíneos se han encontrado depósitos de fibrina; sin embargo, no está claro si puede haber una coagulación intravasal diseminada, pues no siempre hay signos de laboratorio en ese sentido. Se han localizado antígenos antivirales en varios órganos, sobre todo en el hígado, en los riñones, en el bazo y en las hipófisis. En los supervivientes, además, el virus ha sido aislado en la cámara anterior del ojo (hasta 4-5 semanas después de la enfermedad) y en el líquido seminal (hasta la duodécima semana). 4
- 5. Modalidades de contagio La transmisión interhumana es la principal forma de contagio de la gente. Esto ocurre al entrar en contacto cercano con el enfermo. En particular, el contagio se da a través de los líquidos del cuerpo: 1. sangre, 2. saliva, 3. vómito, 4. heces, 5. orina 6. secreciones respiratorias. 7. La transmisión por vía sexual es posible durante varias semanas después de la enfermedad. El pico de máxima infectividad ocurre durante las manifestaciones más graves de la enfermedad, junto con las manifestaciones hemorrágicas. El virus también puede inocularse a través de instrumentos contaminados (fómites). 5
- 6. Diagnóstico El diagnóstico se basa esencialmente en el decurso clínico y en los datos epidemiológicos. Un diagnóstico específico se basa en el aislamiento del virus o bien en la evidencia de la respuesta inmunitaria y en la presencia de material genómico viral. Para probar la presencia de anticuerpos (IgM y IgG) se recurre a un ensayo de inmunofluorescencia indirecta, al uso de la prueba Western blot o de la prueba ELISA. Para distinguir el genoma o los antígenos virales se utiliza la reacción en cadena de la polimerasa (PCR), la inmunofluorescencia, la histoquímica o la prueba ELISA.[2] 6
- 7. Terapia No existe terapia específica. Aunque en la actualidad no existen vacunas o terapias contra los virus del Ébola o Marburgo aprobadas para uso humano, algunos investigadores han conseguido desarrollar vacunas contra ambos patógenos basadas en una forma recombinante del virus de la estomatitis vesicular que produce los virus del Ébola y Marburgo en la superficie de la proteína, y descubrieron que una sola inyección de cualquiera de ambas vacunas en macacos producía respuestas inmunes protectoras cuando el virus correspondiente se introdujo en estos animales. Hay que recurrir a una terapia de apoyo para controlar el volumen hemático, el balance electrolítico y monitorizar atentamente la presencia de infecciones secundarias. Sólo en caso de que se note un estado de coagulación intravasal diseminada, se puede recurrir a la heparina. Se han propuesto terapias a base de suero obtenido de sujetos curados o con interferón, pero actualmente faltan pruebas de apoyo. La ribavirina no ha podido reducir, en experimentos in vitro, la replicación del virus de Marburgo.[1] Es importante el aislamiento del paciente y el uso de dispositivos de protección para el personal médico y enfermeril. Actualmente se realizan estudios para poder crear una vacuna específica.[3] 7
- 8. Resumen Se cree que la fiebre de Marburgo puede ser una zoonosis, pero por el momento todavía no ha sido identificado el depósito del virus, a pesar de que se han tomado en consideración muchas especies animales. Se cree que el virus de Marburgo puede ser endémico en muchas áreas del África Central. Se discute todavía la cuestión de si los filovirus pueden ser responsables de infecciones subclínicas. Todos los grupos de edad son susceptibles de una infección, pero se cree que los más predispuestos son los adultos. Cabe notar, de todos modos, que antes se creía que los niños estaban poco expuestos (8% en la República Democrática del Congo), pero en la epidemia en Angola también ellos resultaron afectados. El 28 de septiembre de 2014 falleció en Kampala, Uganda, un médico radiólogo de 30 años, tras resultar infectado por el virus de Marburgo.[1] 8
- 9. resumen • El virus de Marburgo es capaz de infectar casi todos los órganos (de los linfoides hasta el encéfalo). La transcripción y replicación del virus ocurre en el citoplasma de la célula hospedadora. Se cree que el filamento de ARN se transcribe, gracias a la polimerasa, en una molécula de ARN, complementaria a la nativa, que luego se sobrepone por poliadenilación en la terminal 3’ y, quizás, por inserción de una secuencia externa de la cola 5’. Este ARN se usa después como molde para la traducción y la formación de las proteínas y para la replicación del genoma. • El ingreso del virus a la célula hospedante es mediado por la glicoproteína de superficie, pero no se conoce el receptor al que se pega. Hay quien sostiene incluso que los receptores a los que se pega la glicoproteína pueden ser de distintos tipos. Asimismo, se desconoce si el virus penetra a través de la fusión de la membrana o si a esto se agrega también un proceso de endocitosis. 9
- 10. Resumen 10