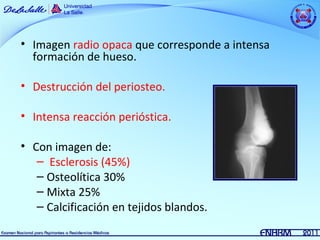
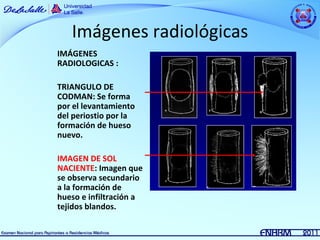
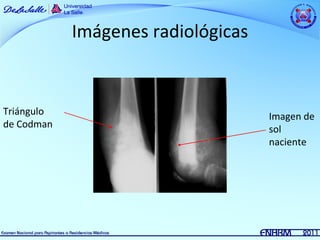
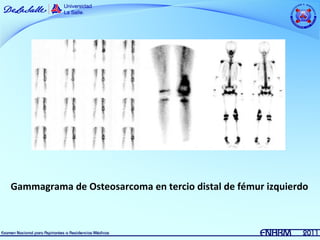
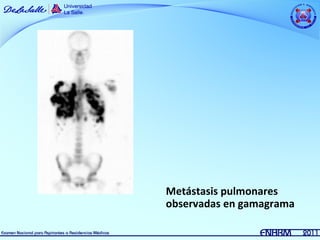
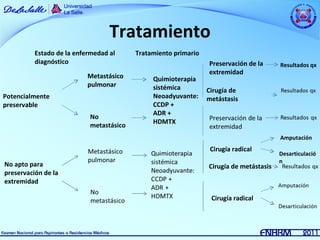
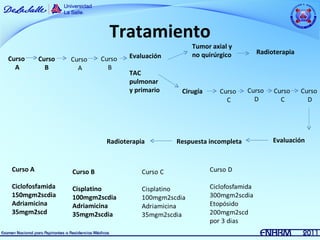
Este documento resume información sobre dos tipos de sarcomas: osteosarcoma y sarcoma de Ewing. El osteosarcoma es el tumor maligno óseo más frecuente en niños y adolescentes, con un pico de incidencia entre los 10-15 años. Se asocia con factores de crecimiento rápido. El tratamiento incluye quimioterapia neoadyuvante, cirugía y quimioterapia coadyuvante. El sarcoma de Ewing es la segunda causa de tumores óseos malignos en niños, que afecta principal