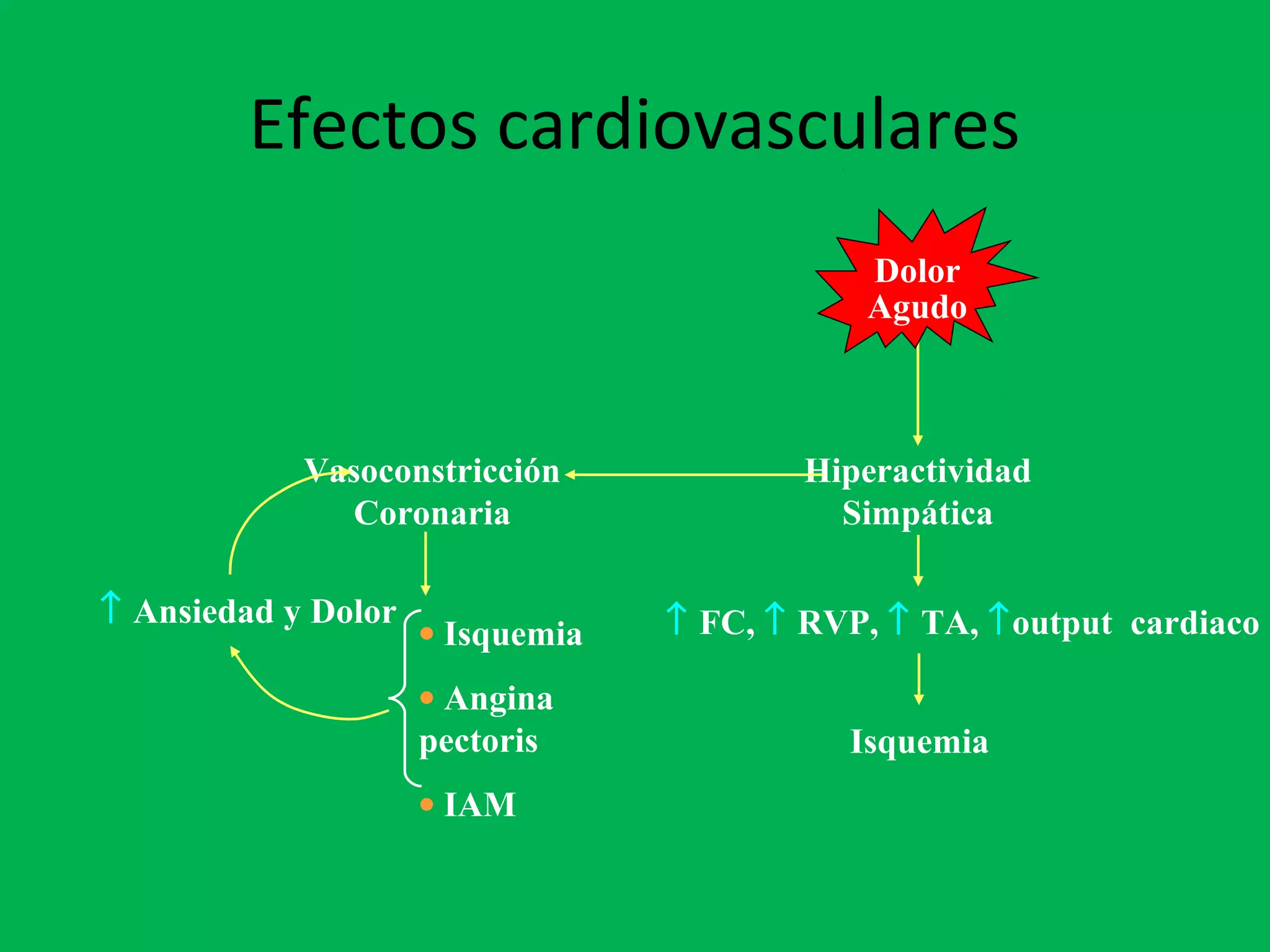
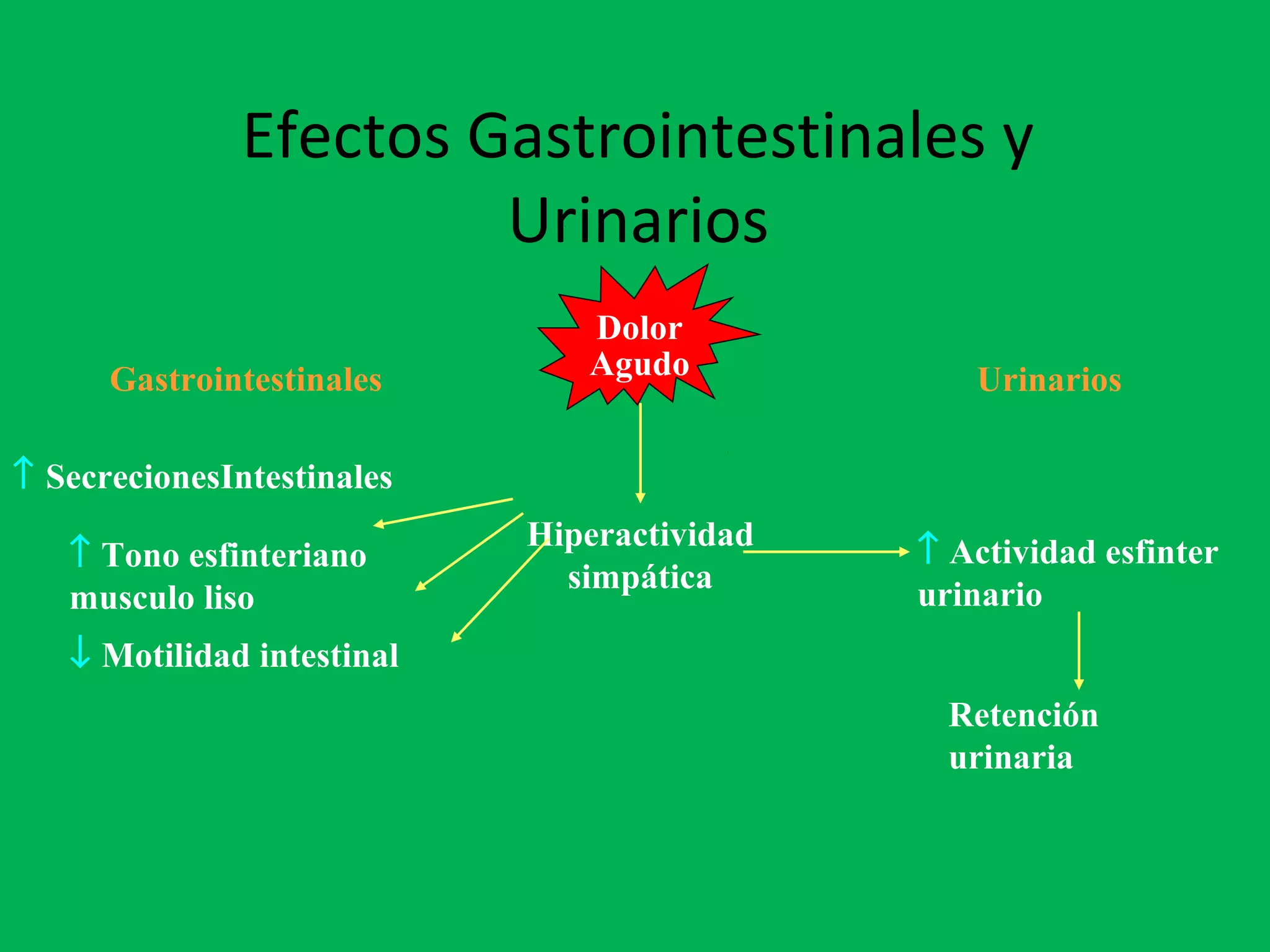
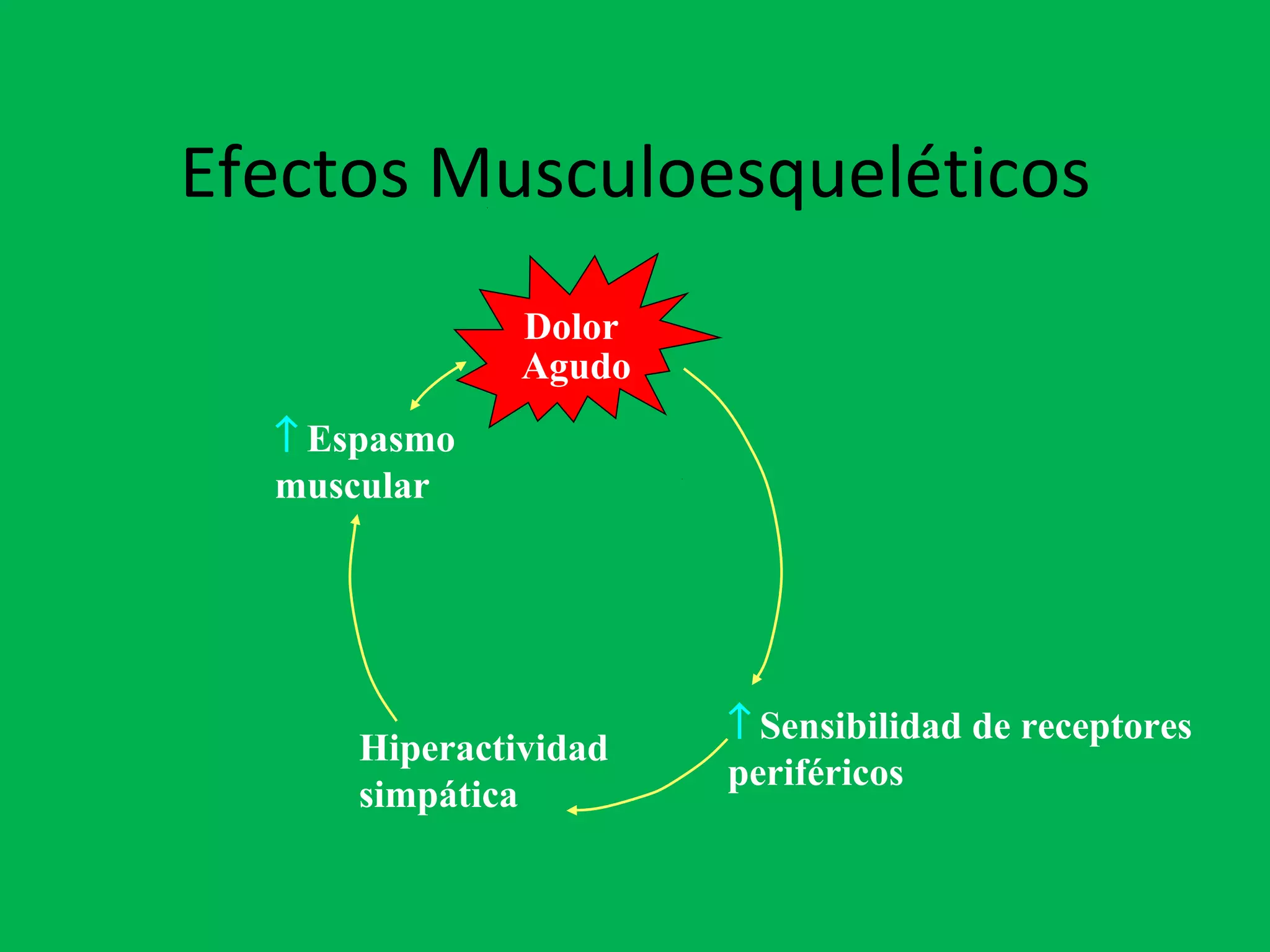
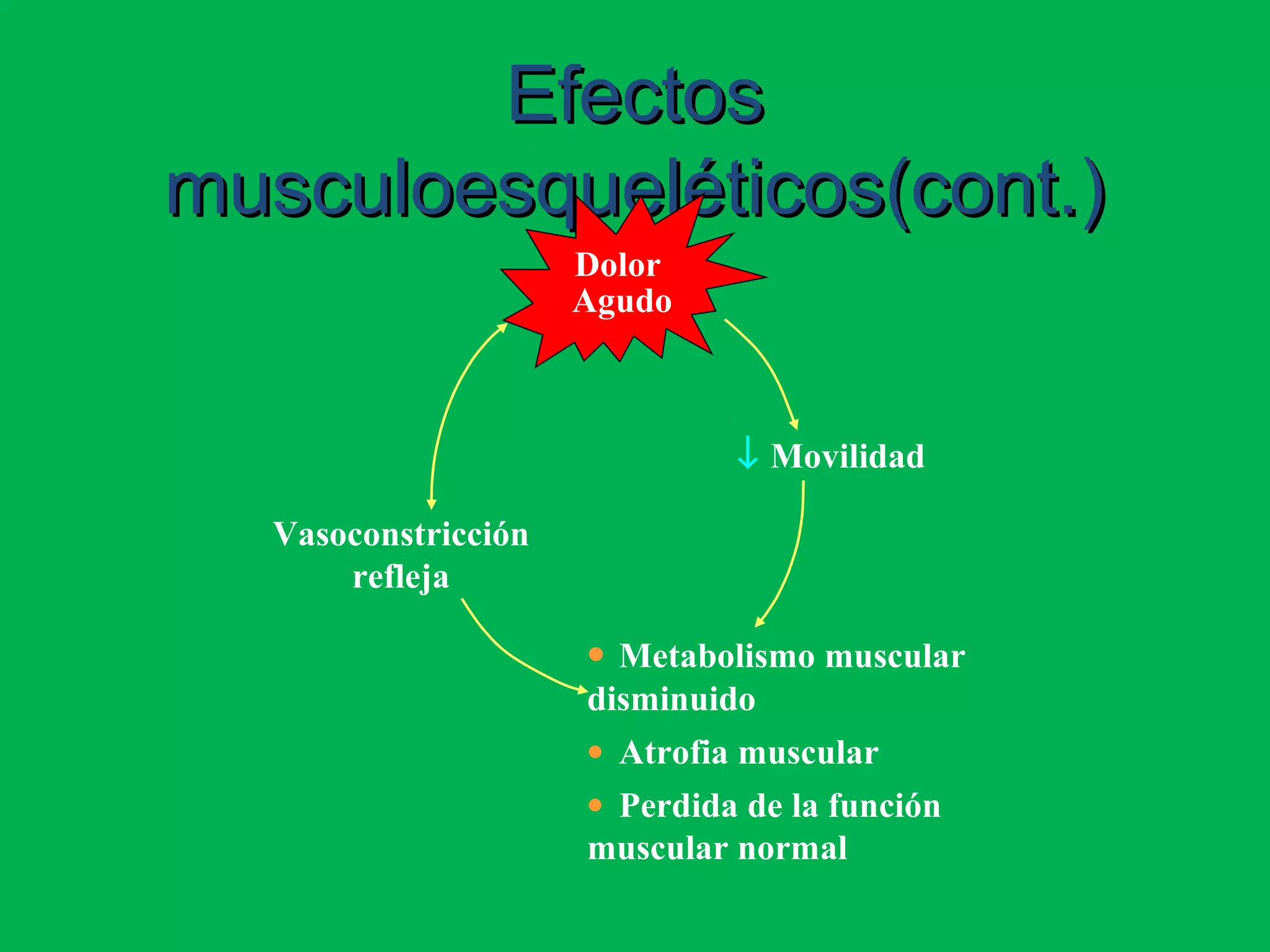
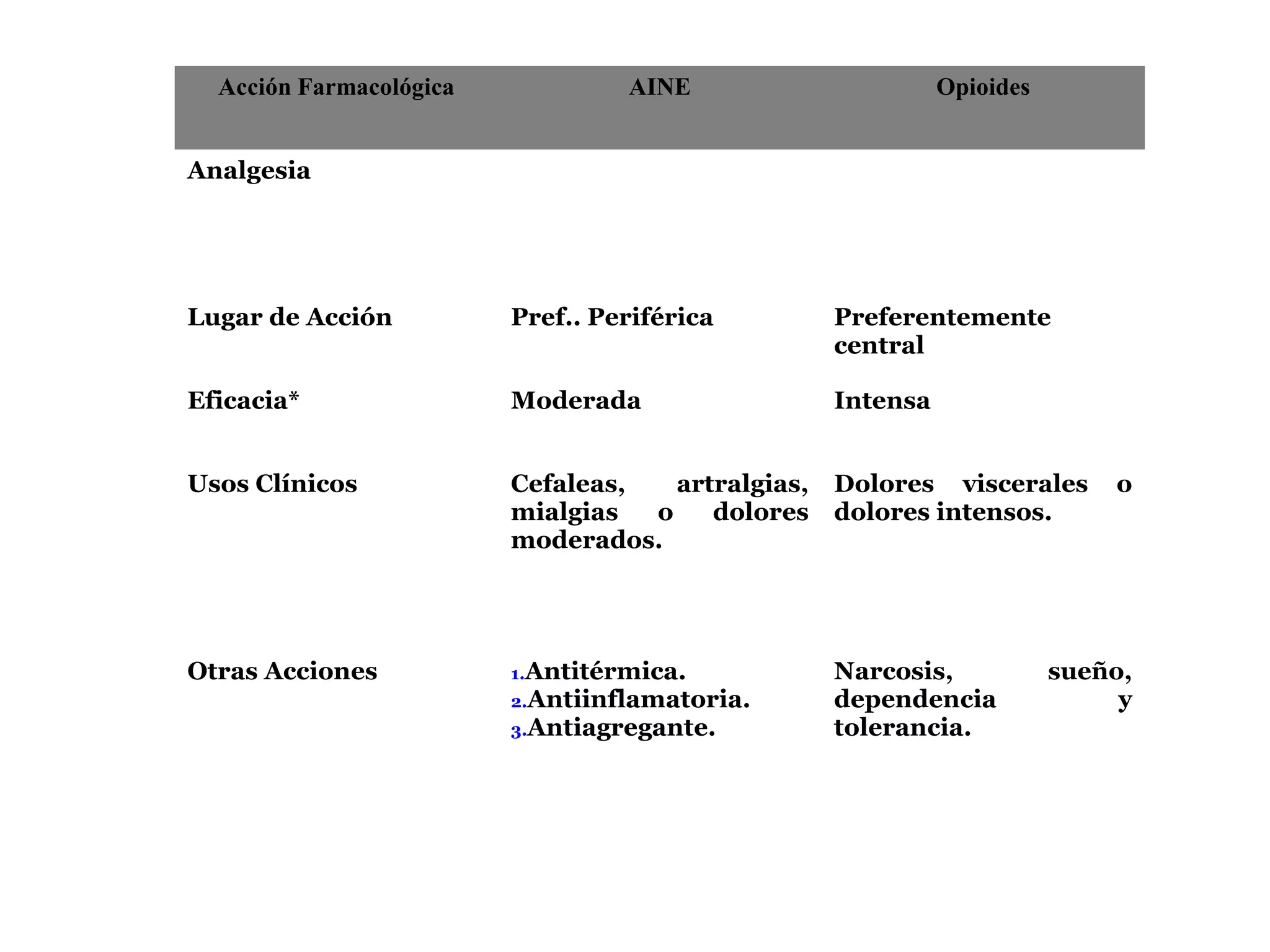
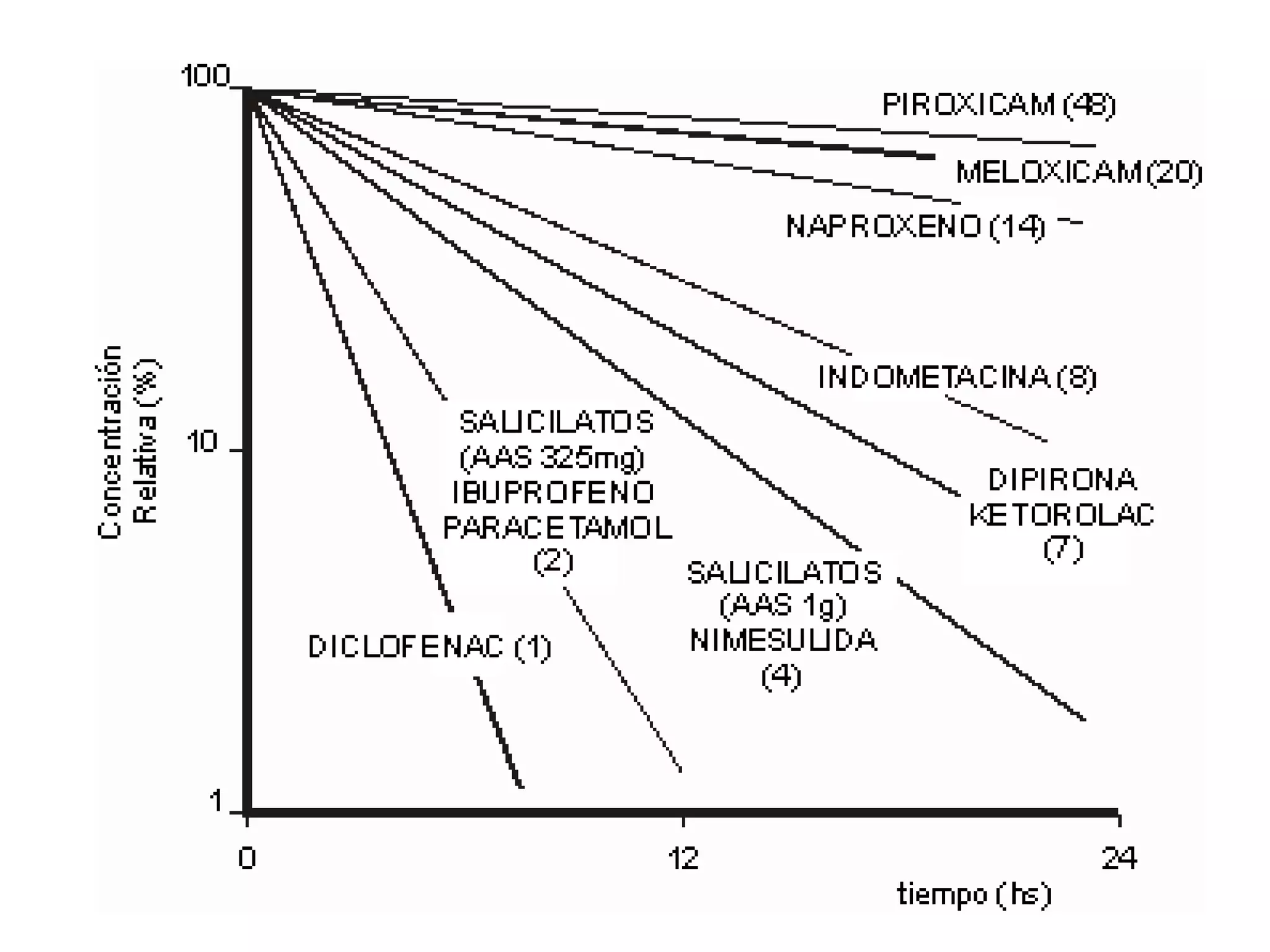
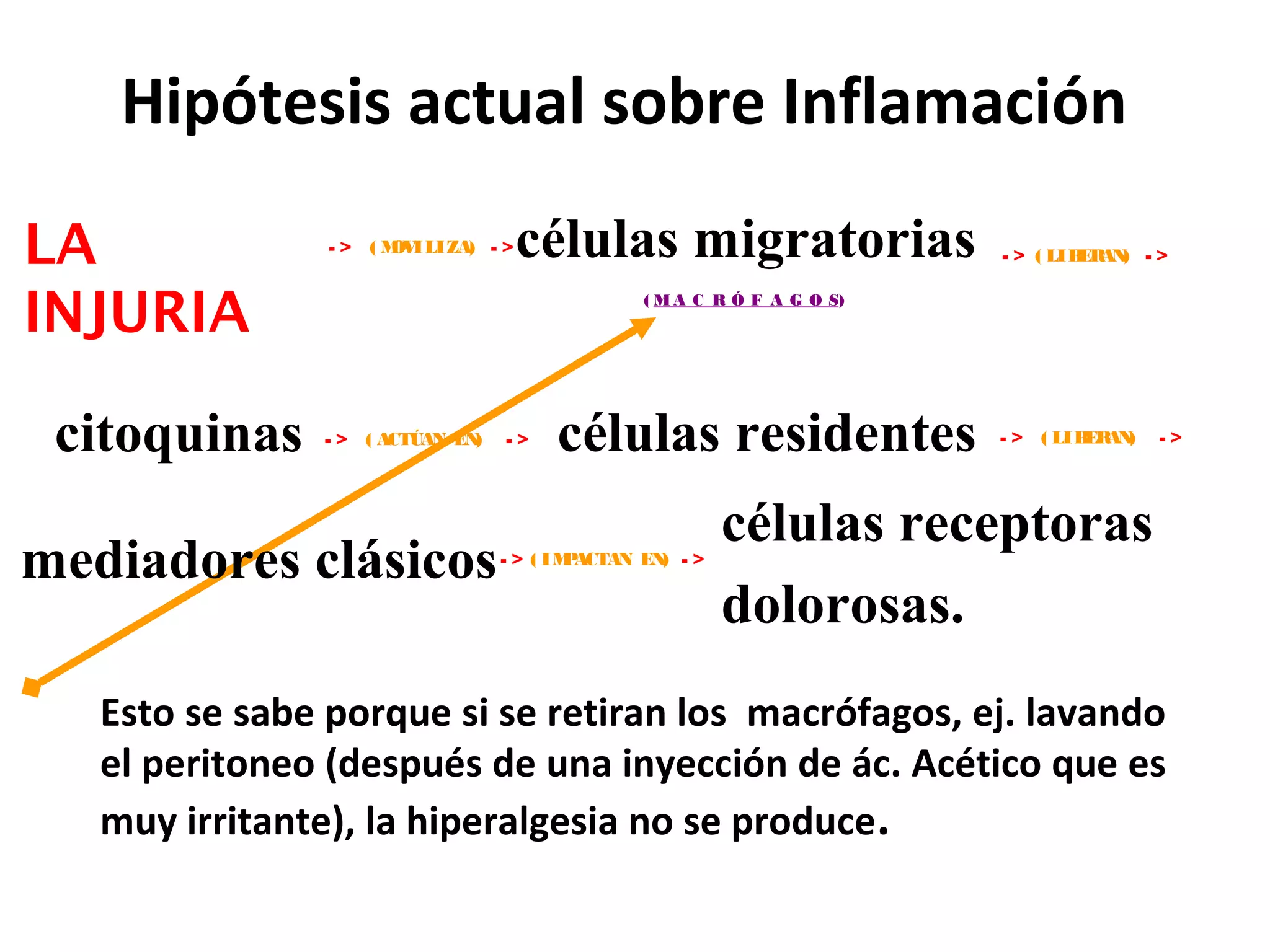
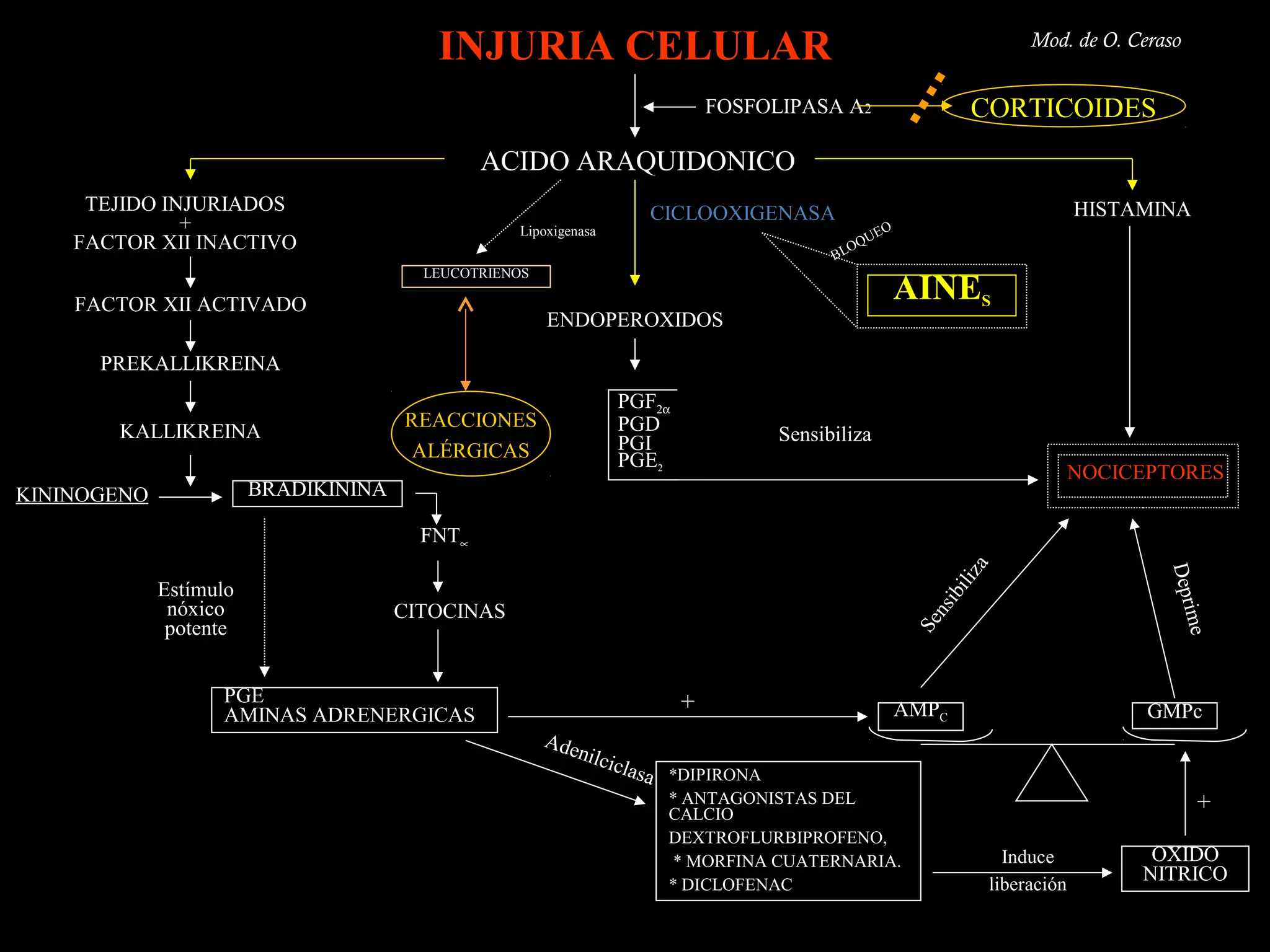
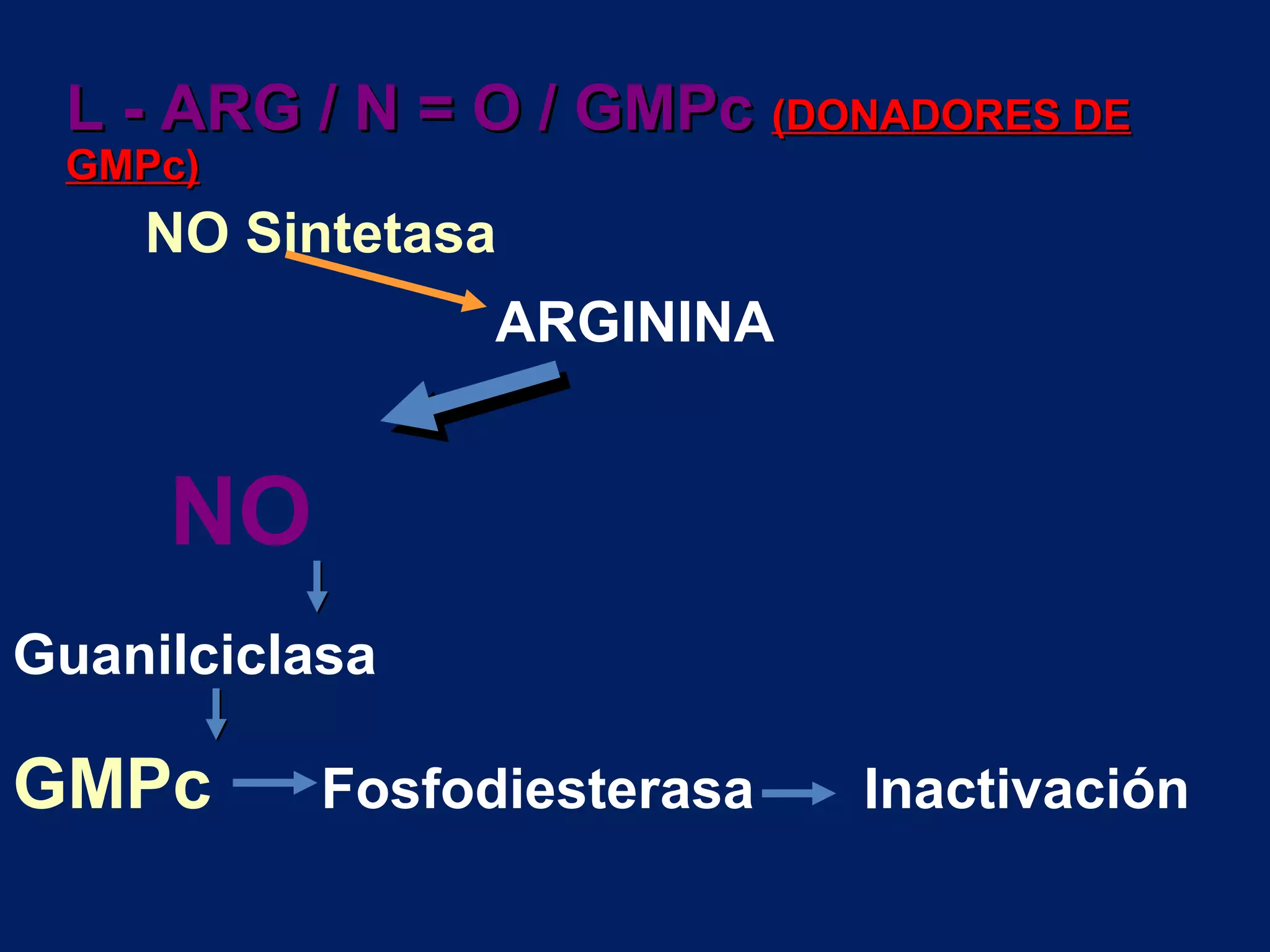
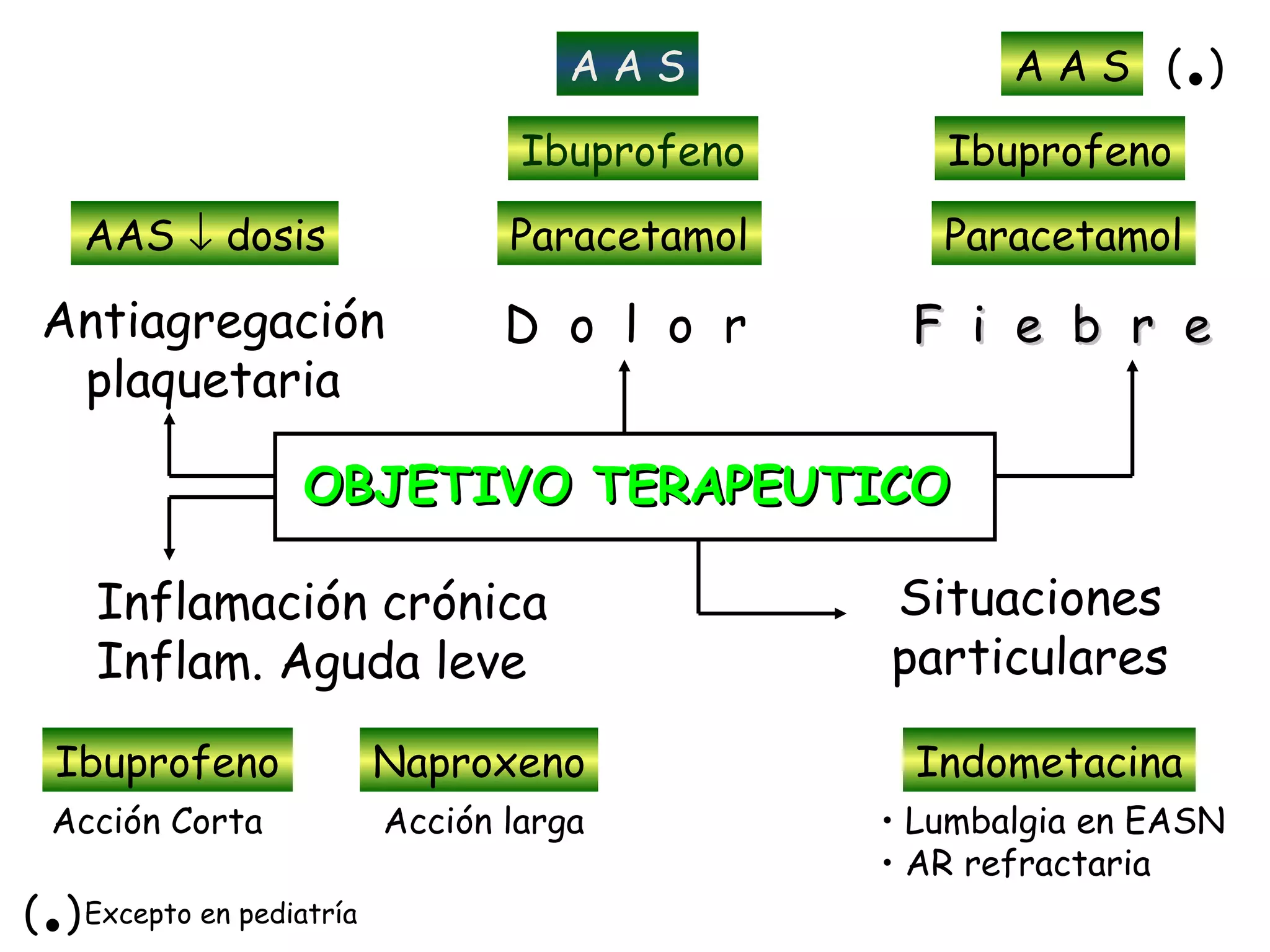
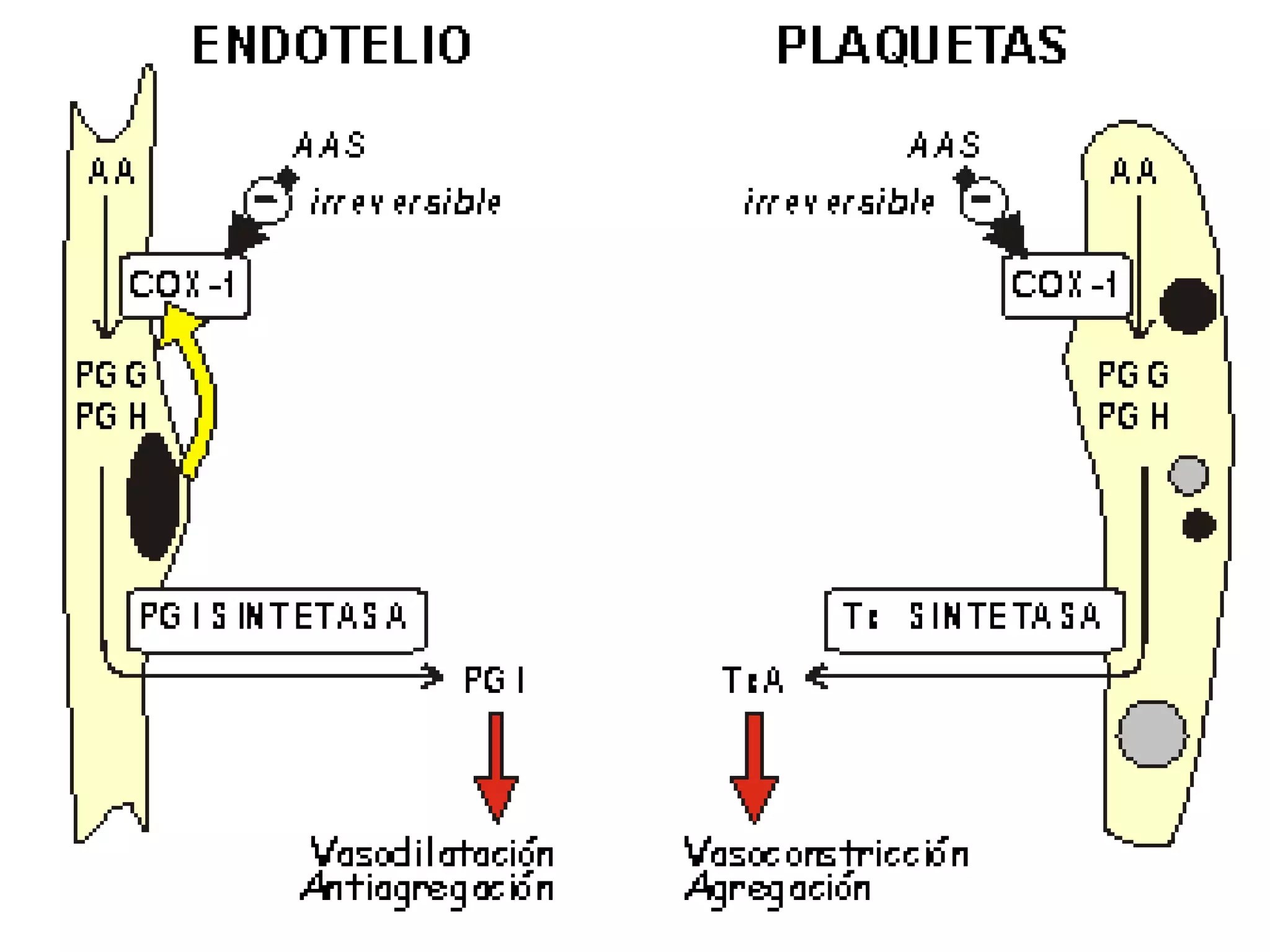
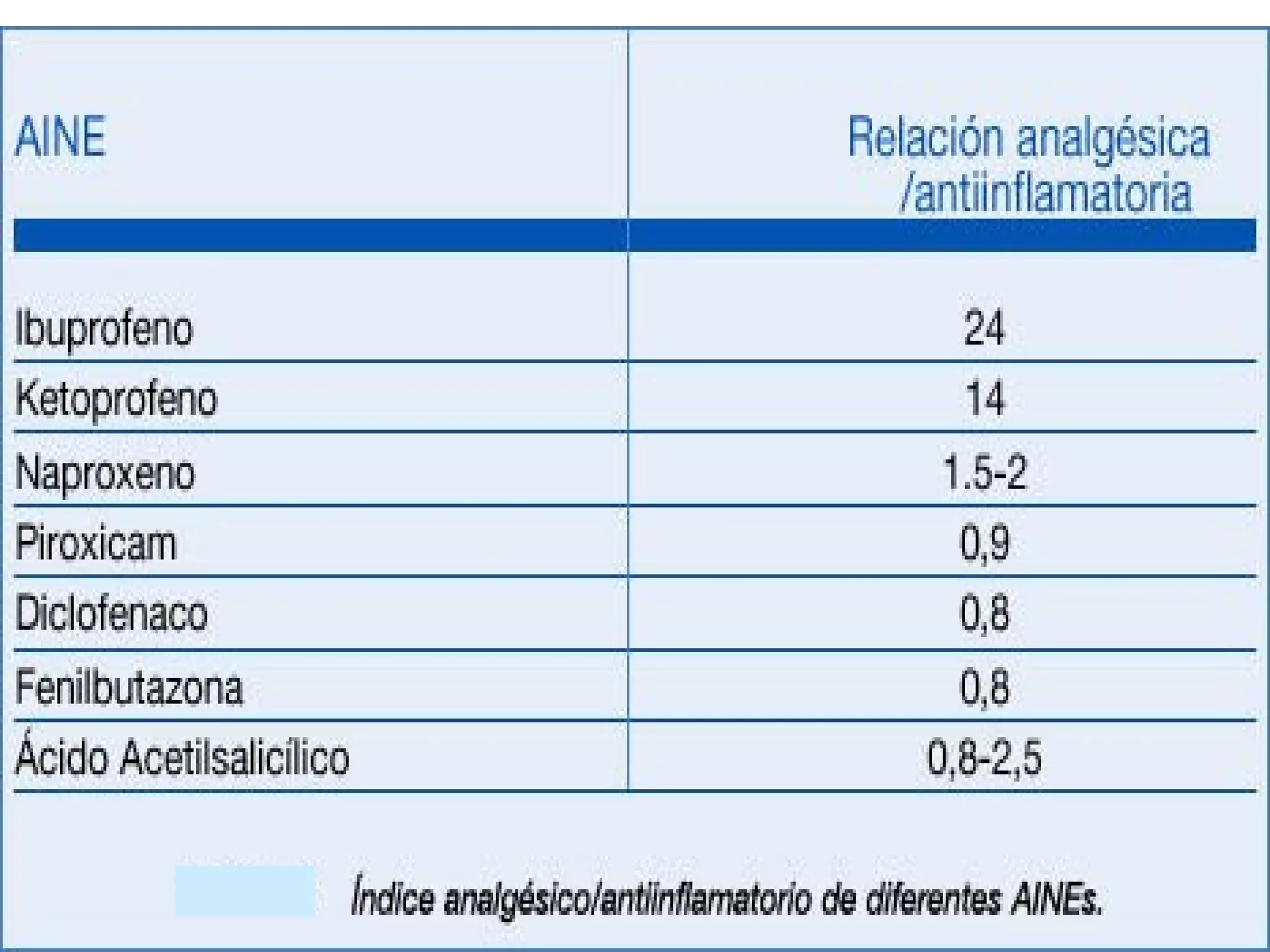
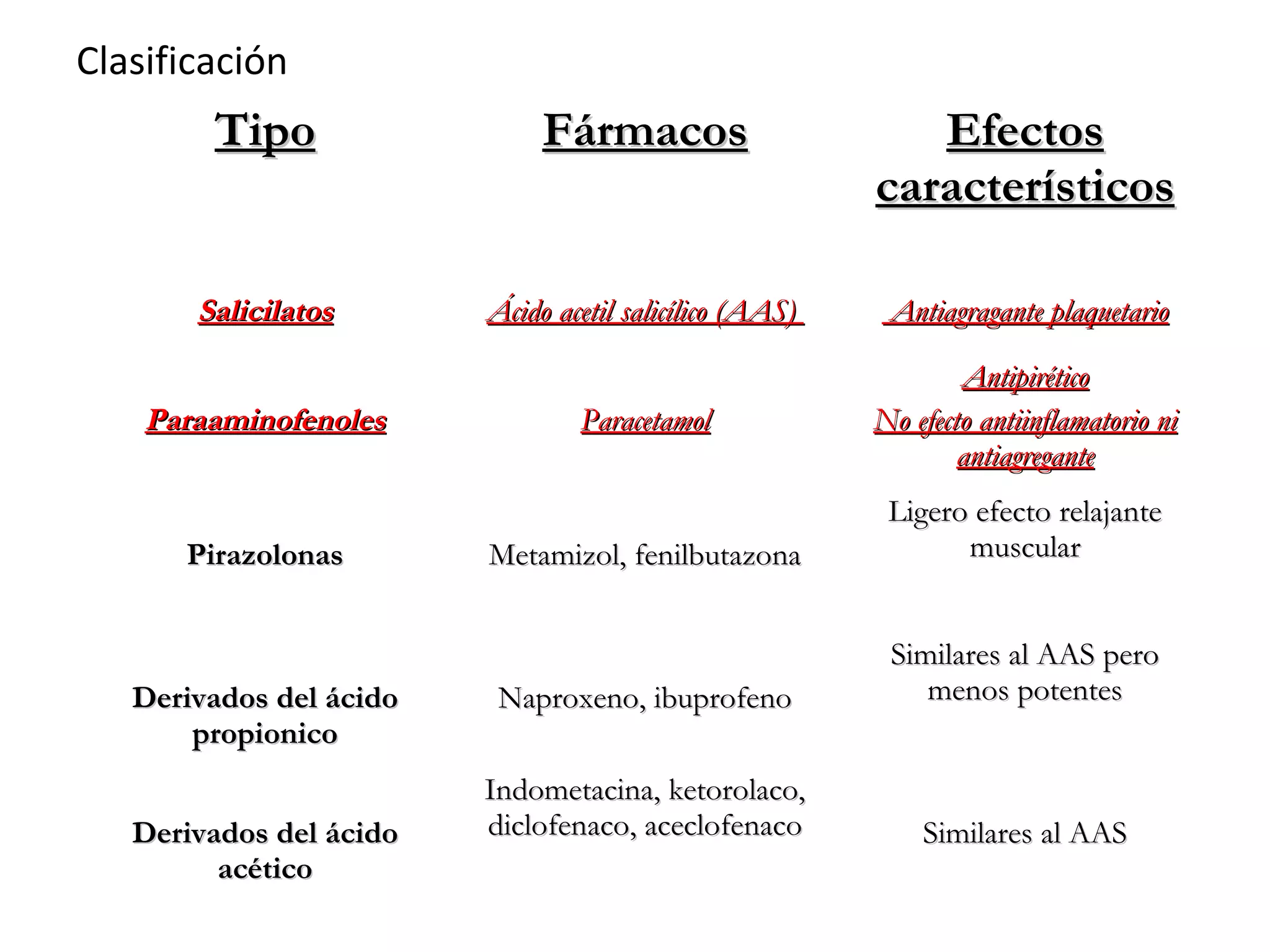
El documento describe las consecuencias fisiológicas del dolor agudo en varios sistemas, incluyendo respuesta neuroendocrina, efectos respiratorios, cardiovasculares, gastrointestinales, urinarios, musculoesqueléticos y psicológicos. También describe los mecanismos de acción periféricos de los AINES, como el bloqueo de prostaglandinas, interferencia con neutrófilos y estimulación de la vía del óxido nítrico.