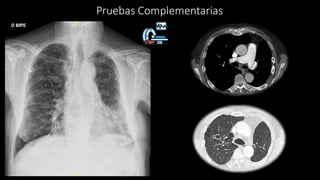
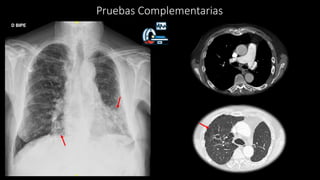
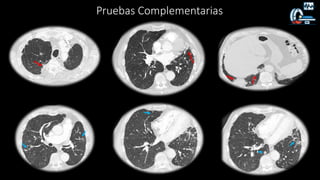
1. Se presenta el caso clínico de un varón de 70 años con bronquiectasias e infección pulmonar recurrente.
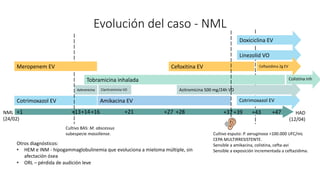
2. Tras varios ingresos y tratamientos antibióticos, se aísla Mycobacterium abscessus subespecie massiliense de un cultivo de esputo.
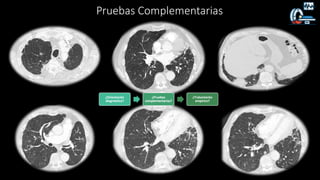
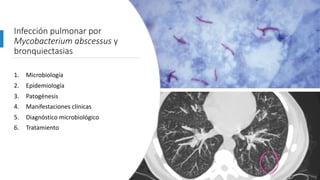
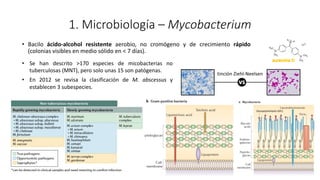
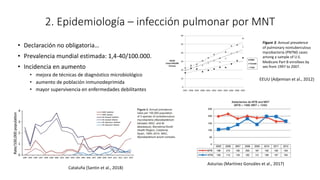
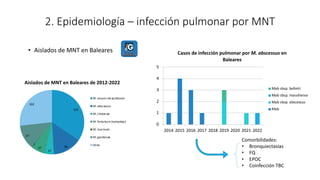
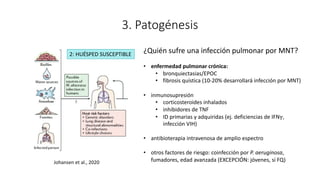
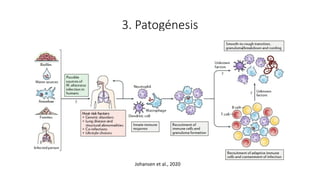
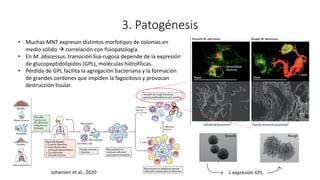
3. El documento proporciona información sobre la microbiología, epidemiología, patogénesis, manifestaciones clínicas, diagnóstico y tratamiento de la infección pulmonar por esta micobacteria.