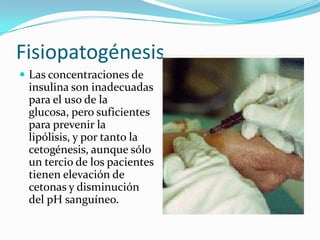
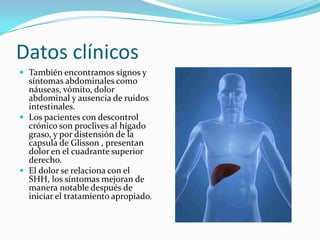
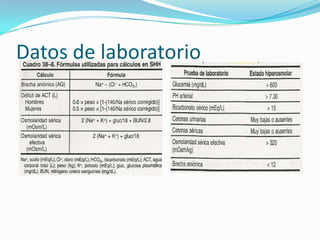
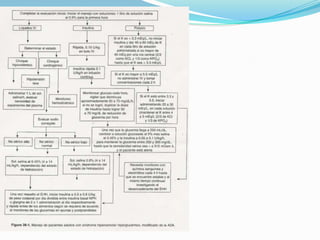
Este documento describe el estado hiperosmolar no cetósico (SHH), una complicación aguda de la diabetes mellitus tipo 2 caracterizada por hiperglucemia superior a 600 mg/dL, deshidratación y ausencia de acidosis cetónica. Explica la fisiopatología, manifestaciones clínicas, hallazgos de laboratorio y tratamiento del SHH, el cual consiste en reposición de volumen y corrección de la hiperglucemia mediante soluciones intravenosas e insulina.




























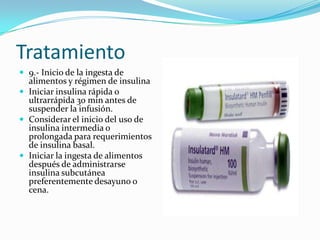
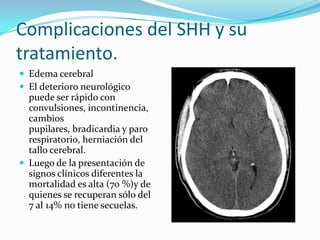
![Tratamiento
5.- Fosfato
A pesar del deficit promedio de fosfatos en estos
pacientes es de 3 a 7 mmol/L, el fosfato sérico puede
encontrarse en cifras normales.
Para evitar fallas musculares por hipofosfatemia y
rabdomiolisis se reponen fosfatos.
Si la [] es < 1 mg/dL. En una reposicion se sugiere
agregarde 20 a 30 mEq/L de fosfato a la solucion que se
este administrando, puede ser como KPO4.](https://image.slidesharecdn.com/estadohiperosmolarnocetsico-120311235921-phpapp01/85/Estado-hiperosmolar-no-cetosico-35-320.jpg)