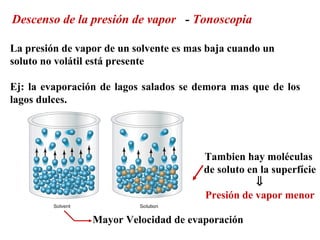
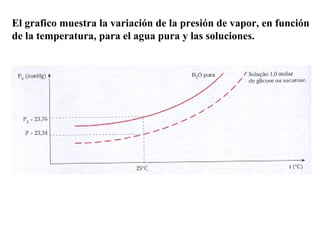
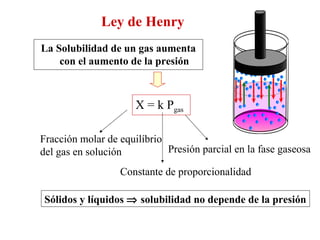
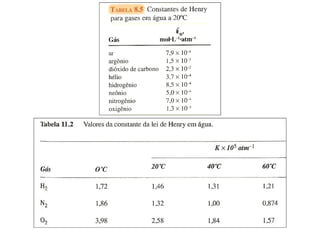
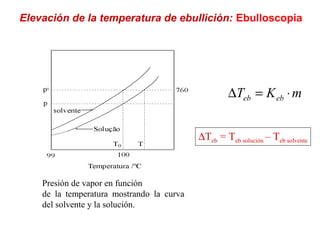
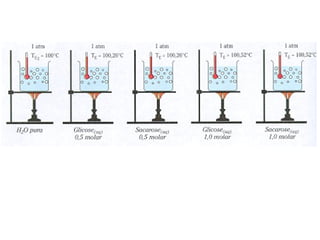
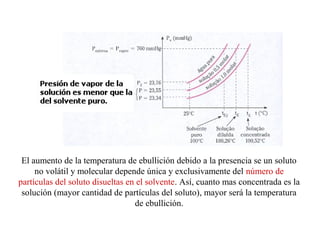
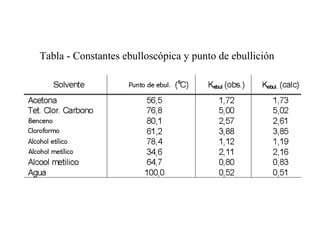
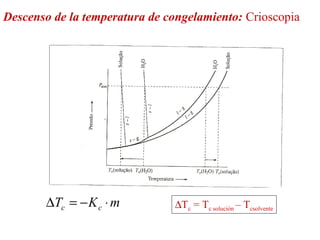
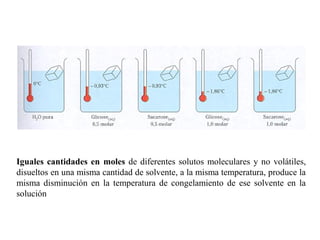
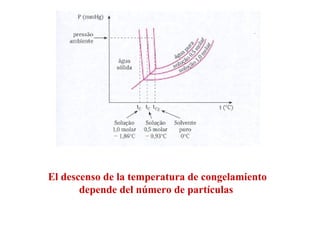
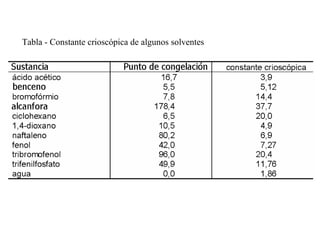
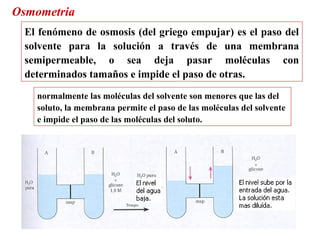
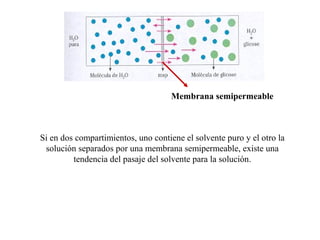
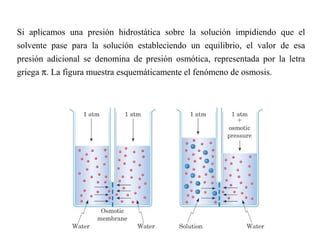
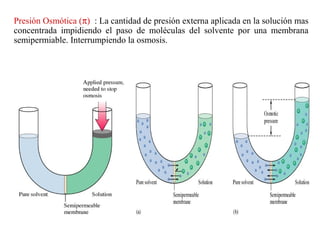
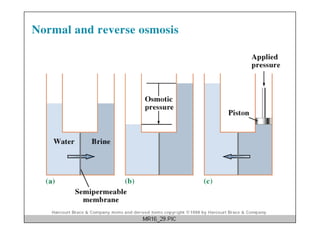
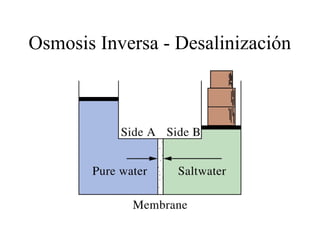
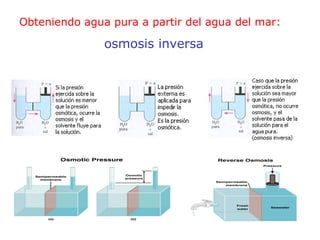
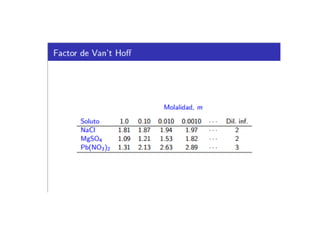
El documento detalla conceptos de coligativos como descenso de presión de vapor, aumento del punto de ebullición y descenso del punto de congelamiento, así como el fenómeno de osmosis y presión osmótica. Se describen las leyes de Raoult y Henry para soluciones ideales y el análisis de la presión osmótica en soluciones diluidas, junto con aplicaciones prácticas. Además, se proponen ejercicios de cálculo relacionados con la disolución de sustancias y sus propiedades coligativas.