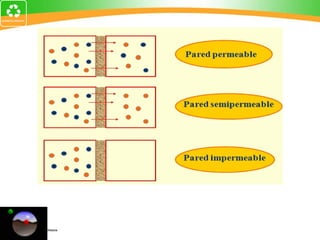
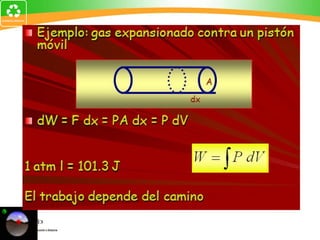
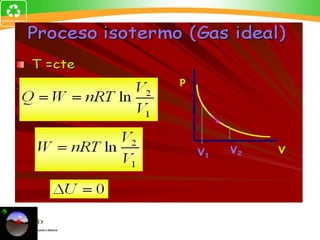
Este documento presenta información sobre procesos termodinámicos y sistemas cerrados, abiertos y aislados. Explica que el cambio de estado ocurre a través de la variación de propiedades termodinámicas y solo mediante procesos termodinámicos. Luego, propone cuatro problemas que involucran el cálculo de trabajo, energía y calor para procesos de expansión reversible, isobáricos e isotérmicos de gases. Finalmente, concluye sugiriendo aplicaciones de la termodinámica en refrigeración