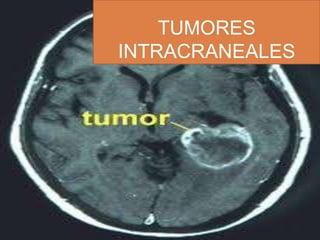
Tumores Intracraneales
- 2. Epidemiología Los tumores cerebrales representan la segunda causa de muerte por afecciones del sistema nervioso. 10 mil casos por cada 100 mil habitantes. CBTRUS, 1998 Central Brain Tumors Registry
- 3. Epidemiología Factores Genéticos. Ocupacionales y Ambientales. Sustancias Químicas. (Plásticos y Caucho).
- 4. Causas y factores de riesgo Ambientales Genéticos: mutación en un gen específico pasada de abuelos a padres y a los hijos Neurofibromatosis 1 y2 Esclerosis tuberosa
- 6. FRONTAL
- 8. TEMPORA L
- 9. OCCIPITA L
- 10. Tumores cerebrales de importancia clínica CLASIFICACIÓN DE LOS Histológicamente benignos o malformativos TUMORES Meningiomas Adenomas pituitarios CEREBRALES / CLASSIFICA Neurinomas del acústico TION OF TUMOURS OF THE Craneofaringiomas Astrocitomas pilocíticos CENTRAL NERVOUS Tumores epidermoides SYSTEM Quistes coloides Tumores cerebrales primarios • • • • • • • •Papilomas de los plexos coroideos •Hemangioblastomas Histologicamente malignos Gliomas Neoplasias astrogliales Astrocitomas* Astrocitomas anaplásicos Glioblastomas multiformes Oligodendrogliomas Gangliomas* Ependimomas Linfomas Meduloblastomas Tumores neuroectodérmicos primitivos Tumores de células germinales Tumores de células pineales Cordomas Carcinomas del plexo coroide Tumores cerebrales metastásicos Metastasis únicas o múltiples Carcinomatosis meníngea
- 11. Tumores cerebrales primarios Los glioblastomas multiformes Los astrocitomas Los meduloblastomas Ependimomas
- 12. Biología y Desarrollo Tumoral DNA dañado Mutación espontanea o por interacción de agentes químicos o ambientales. El desarrollo tumoral depende del equilibrio entre la proliferación y la perdida celular.
- 13. Incidencia por Edad y Sexo 54 años Tumores Intracraneales. (Promedio) Tipo de Neoplasia Incidencia (Años) Meningiomas (Femenino 80%) 75 + Astrocitomas 65 a 75 Oligodendrogliomas 35 a 45 CBTRUS
- 14. Incidencia Tumores Primarios Tumores Secundarios 50 % y 70% (General) 80% en los hemisferios Cerebrales Masculino 1,7/1 Incidencia vs Mujeres 10% y 15% Cerebelo Gliomas 40% a 60% 3% y 5% Tronco Cerebral. Meningiomas 10% a 30%
- 15. Presentacion Clinica Se encuentran Confinados a un espacio Limitado. Sx de Hipertension endocraneana Mareos Alteraciones Psiquicas y de la Concencia. Diferente Topografia Lesional. Crisis Convulsivas
- 16. Gioblastoma Multiforme Gioblastoma Primario o de “de Novo”. Gioblastoma secundario. Gioblastoma Primario Gioblastoma Secundario 5 y 6 Década de la Vida Pacientes mas Jovenes. Amplificacion o sobreexposicion de EGFR Alteracion Genetica p53 Comportamiento supratentorial.
- 17. Clinica Compresión vascular. Bloqueo de la circulación del liquido cefalorraquídeo. Destrucción parenquimatosa. En un 30% de los casos pueden presentar crisis epilépticas. Alteraciones Psiquiátricas. Hidrocefalia.
- 18. Pronostico Es sombrío. Supervivencia media es de 52 Semanas (1 año 1 mes). El tratamiento según su localización y extensión, es cirugía precedida e Quimioterapia (temozilamida) y Radioterapia. Despues del tratamiento la vida media es de 8 a 12 meses.
- 19. Metástasis Cerebral Son los tumores intracraneales más frecuentes. 10% al 15% de los pacientes con cáncer tendrán metástasis cerebrales, aunque en los estudios de autopsias se han encontrado metástasis cerebrales hasta en 20% a 40% de los pacientes.
- 22. glioma de bajo grado tumores curables quirúrgicamente glioma más común en los niños representa 10% de los tumores astrocíticos cerebrales 85% de los cerebelares Ambos sexos lento crecimiento = volúmenes importantes
- 24. Ubicaciones más comunes: nervio óptico quiasma óptico cerca del hipotálamo el tálamo los ganglios basales los hemisferios cerebrales el cerebelo
- 25. El término“anaplásico” se utiliza cuando el tumor ha desarrollado un amplio suministro de sangre alrededor de sí mismo o cuando el tumor contiene células muertas.
- 26. Síntomas Acompañan al paciente a lo largo de varios meses Variados Dependen de la edad del niño y la ubicación del tumor. Pérdida de equilibrio, dificultad para caminar, deterioro de la escritura y trastornos del habla.
- 27. También cefaleas matinales asociadas a vómitos Modificaciones de la personalidad o conducta, que pueden ser muy sutiles, como somnolencia inusual o cambios en el nivel de energía Cambios inexplicables del peso corporal.
- 28. Dx La RM con contraste examen ideal por que permite certificar la extensión y características del tumor para realizar la planificación quirúrgica. Biopsia intraoperatoria que permite contar con un diagnóstico histopatológico que confirme el diagnóstico imagenológico.
- 32. Tratamiento Resección quirúrgica completa 70% de los pacientes excepto en vía óptica e hipotálamo la posibilidad de resecar completamente el tumor es proporcional a la precocidad del diagnóstico. 90 - 94% de sobrevida libre de enfermedad a 10 años glioma de mejor pronóstico.
- 33. Resección incompleta: tratamiento adyuvante La radioterapia en adultos y niños mayores de 10 años. La quimioterapia niños mas pequeños. Los tumores más sensibles a la quimioterapia son los astrocitomas pilocíticos y los astrocitomas anaplásicos.
- 34. MEDULOBLASTOMA Representan13% de los tumores cerebrales en menores de 14 años Representan el 20% de los tumores cerebrales en adultos siempre se localizan en el cerebelo.
- 35. De crecimiento rápido Se propaga a otras partes del SNC Se puede propagar dentro del cuarto ventrículo y bloquear la circulación del LCR o enviar células tumorales hasta la médula espinal No es común que los meduloblastomas se propaguen fuera del cerebro y la médula espinal.
- 36. Síntomas cambios en el comportamiento (niños pequeños) Síntomas de aumento de la PI como: Dolores de cabeza Náuseas y vómitos Somnolencia Falta de equilibrio al andar Mala coordinación de las extremidades Movimientos inusuales de los ojos.
- 37. Tratamiento Extirpación quirúrgica de la mayor cantidad de tumor posible Radiación y quimioterapia Pruebas para verificar una posible propagación del tumor: RM de la médula espinal análisis del LCR
- 38. Pasos a seguir después de la cirugía: Radiación en el área del tumor seguida por una dosis baja de radiación en todo el cerebro y la médula espinal. después de la radioterapia se administra quimioterapia Los niños muy pequeños suelen tratarse con quimioterapia en lugar de radiación para aplazar su uso hasta que sean mayores.
- 39. Los agentes más usados son una combinación de cisplatino y vincristina ya sea con ciclofosfamida o CCNU No existe un tratamiento estándar para los tumores recidivantes. Buena respuesta a quimioterapia=dosis alta con autotrasplante de células madre.
- 40. Gracias Por su Atención.
