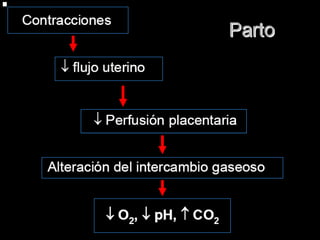
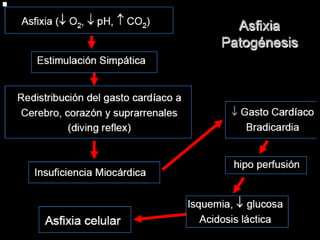
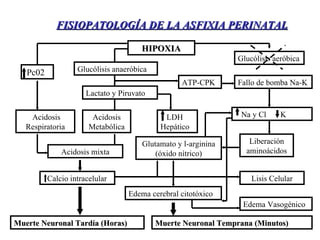
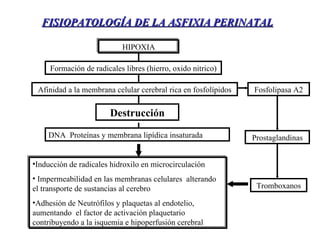
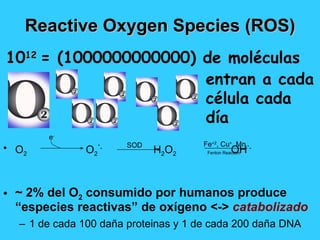
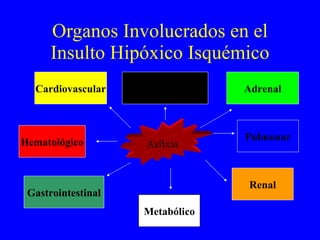
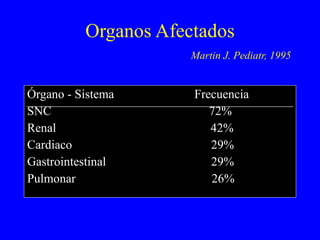
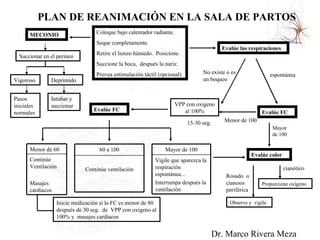
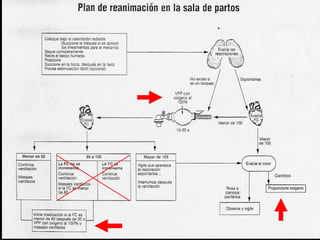
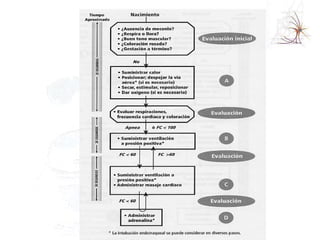
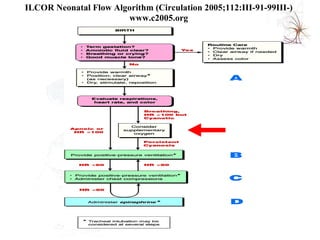
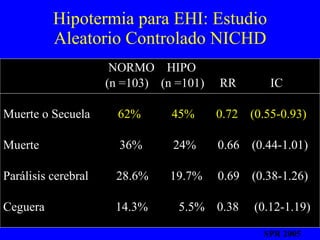
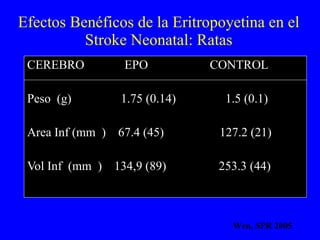
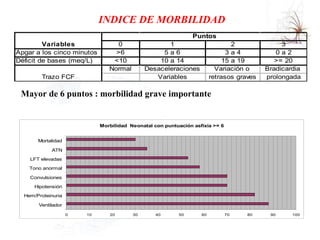
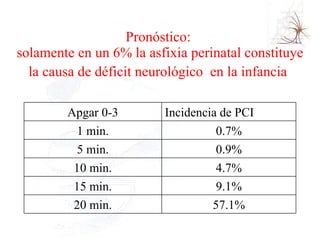
El documento proporciona información sobre asfixia perinatal, incluyendo definición, criterios clínicos, factores de riesgo, mecanismos, efectos en diferentes órganos y sistemas, y recomendaciones para la reanimación del recién nacido asfixiado, con énfasis en el uso de oxígeno puro versus aire durante el proceso de reanimación.