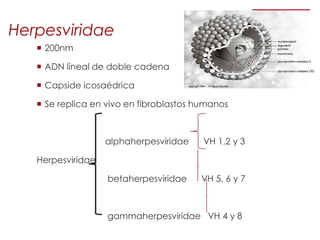
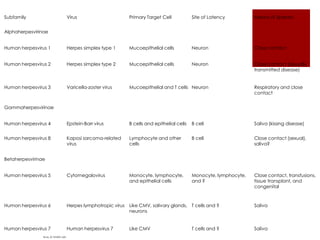
El documento describe el citomegalovirus humano (herpesvirus 5), uno de los herpesvirus más comunes que causa infección congénita. Se replica en células epiteliales, macrófagos, linfocitos y otras células, estableciendo latencia en linfocitos T, macrófagos y otras células. Se transmite a través de la sangre, el tejido y la mayoría de las secreciones corporales.