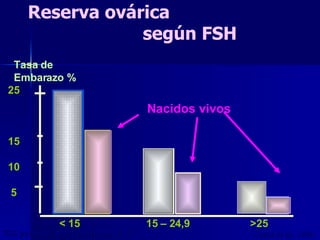
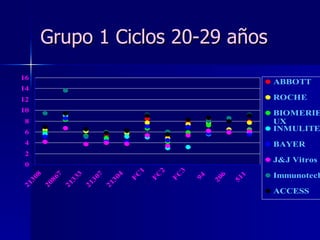
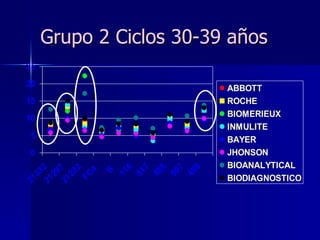
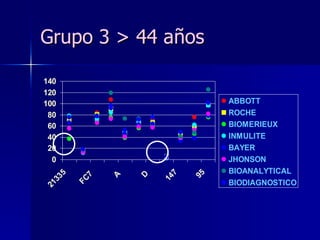
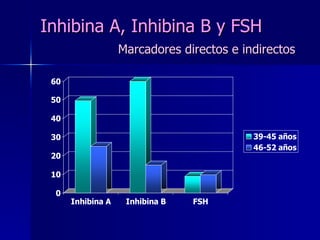
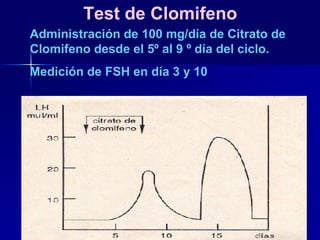
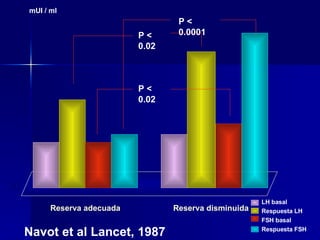
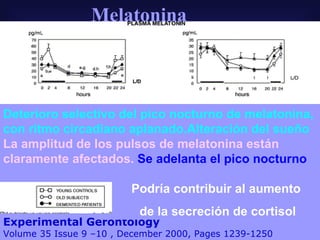
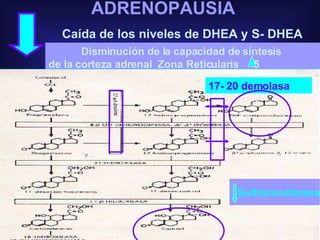
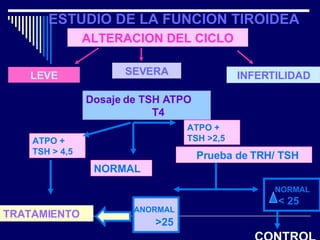
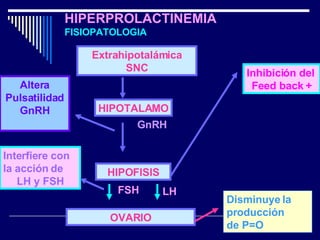
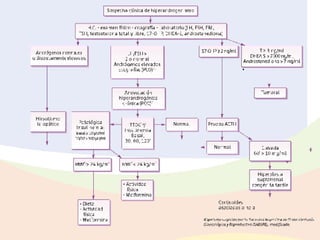
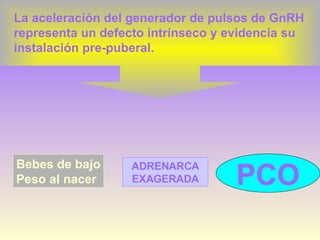
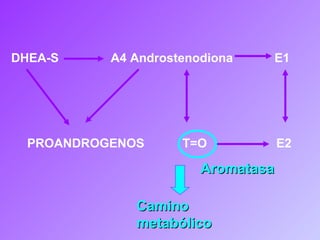
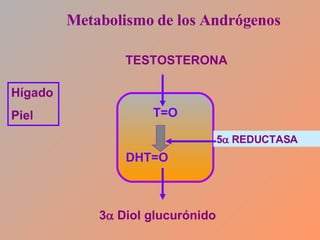
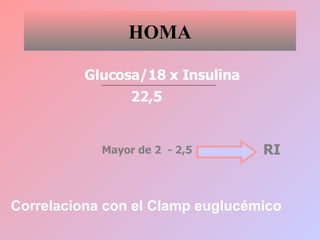
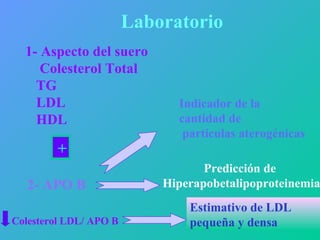
Este documento trata sobre los biomarcadores del envejecimiento reproductivo y ovárico. Explica las teorías del envejecimiento como el declive de la telomerasa, el reloj biológico y los radicales libres, y cómo afectan a la fertilidad con la edad. También describe biomarcadores como la FSH, la AMH, y la Inhibina B para evaluar la reserva ovárica, y cómo sus niveles cambian con la edad prediciendo la calidad ovárica y la respuesta a la estimulación.