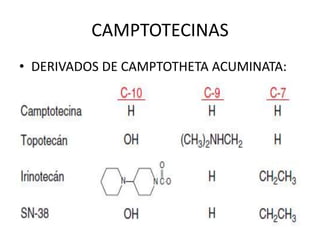
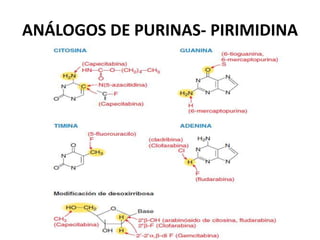
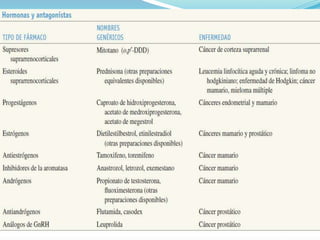
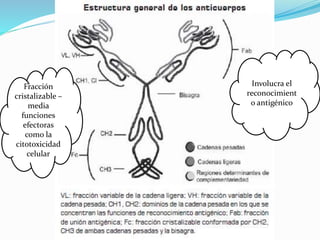
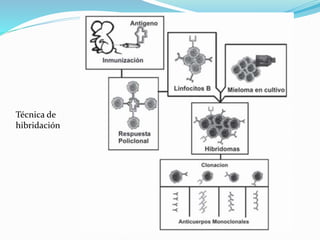
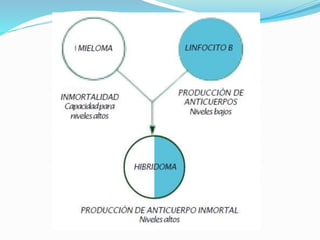
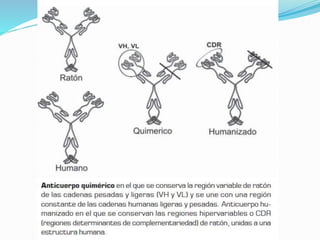
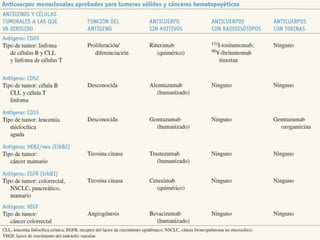
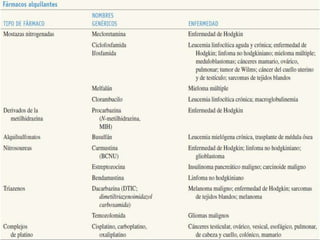
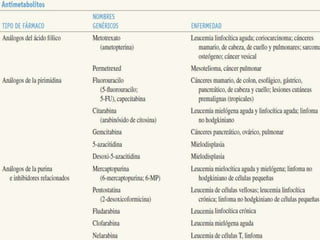
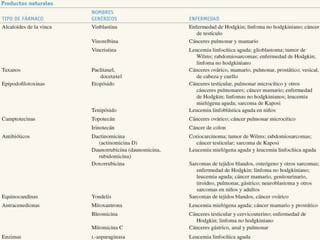
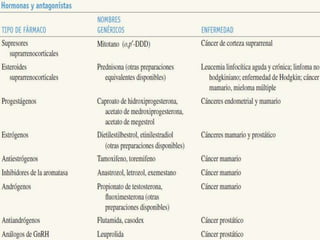
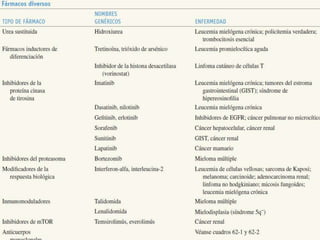
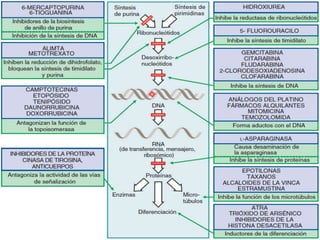
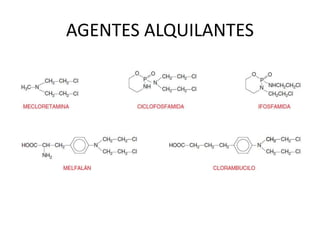
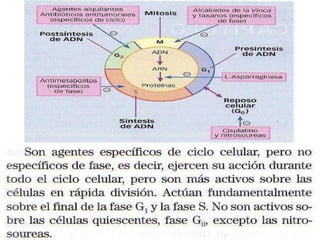
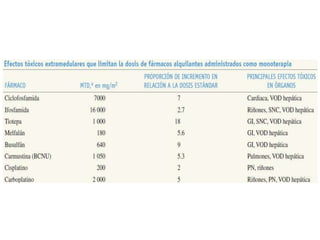
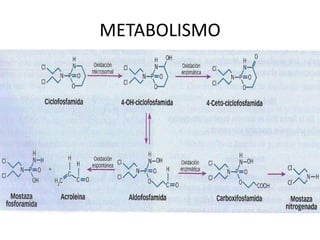
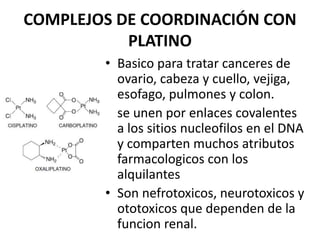
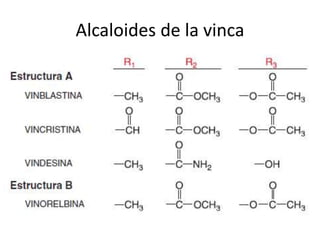
El documento describe los principales tipos de antineoplásicos, incluyendo sus mecanismos de acción, usos terapéuticos y efectos adversos. Explica las fases del ciclo celular y los principios del tratamiento con antineoplásicos. Luego describe varios agentes como los alquilantes, los complejos de platino, las nitrosureas y los alcaloides de la vinca, detallando sus propiedades farmacológicas.







































![toxicidad
• El paclitaxel afecta la medula ósea. Ocho a 11 días después
el filgrastim [factor estimulante de colónias de granulocitos
(G-CSF, granulocyte-colony stimulating factor)], son toleradas
adecuadamente dosis incluso de 250 mg/m2 en un lapso de
24 h.
• neuropatia periferica se torna un trastorno que limita la
dosis.
• Muchas personas presentan mialgias durante varios dias
despues de recibir el paclitaxel.
• En esquemas de altas dosis o con uso prolongado la
neuropatia sensitiva en guante- calcetin puede ser
discapacitante,
• La mucositis es notable en el caso de infusion intravenosa
durante 72 a 96 h y en el esquema semanal.](https://image.slidesharecdn.com/antineoplasicos-180627190625/85/Farmacologia-Antineoplasicos-58-320.jpg)