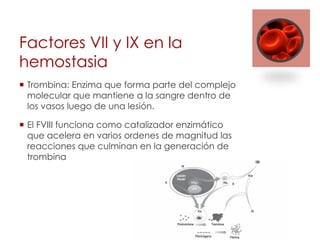
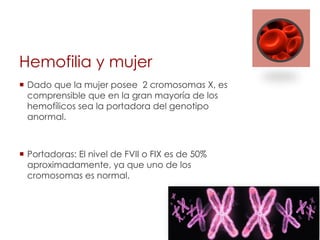
La hemofilia es un trastorno genético ligado al cromosoma X que causa un defecto en los factores de coagulación VIII o IX. Esto conduce a hemorragias espontáneas o traumáticas prolongadas. La hemofilia A se debe a la deficiencia del factor VIII y es la forma más común, mientras que la hemofilia B implica la deficiencia del factor IX. El tratamiento consiste en la reposición del factor deficiente para prevenir hemorragias y daño articular a largo plazo.


























![Tratamiento en pediatría
¡ FVIII: Peso x [ nivel deseado del factor x (0.5) ]
¡ El resultado indica el número de unidades requeridas del factor
por dosis.](https://image.slidesharecdn.com/hemofilia-170401191541/85/Hemofilia-29-320.jpg)

