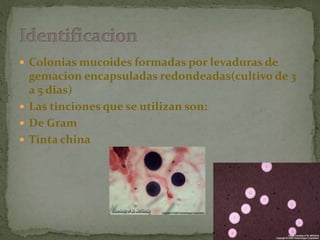
1. La histoplasmosis es una infección micótica causada por el hongo dimorfo Histoplasma capsulatum que se adquiere por inhalación y afecta principalmente los pulmones.
2. Tiene distribución cosmopolita pero es endémica en regiones tropicales y templadas de América.
3. Los síntomas van desde asintomático hasta neumonía aguda, y puede diseminarse a otros órganos en personas inmunocomprometidas.