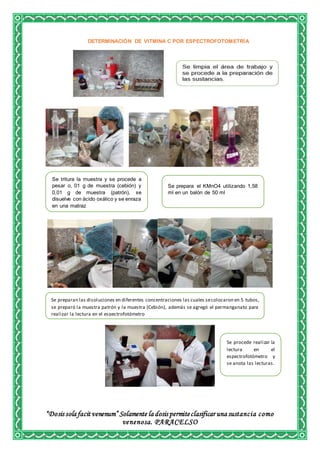
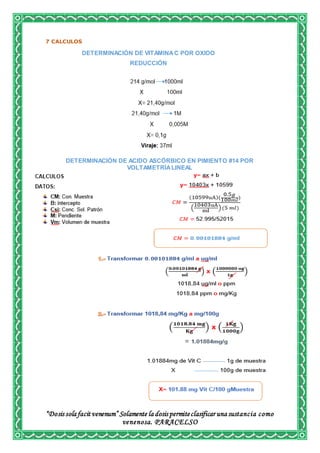
Este documento describe los procedimientos realizados en un laboratorio para evaluar la calidad de la vitamina C a través de diferentes ensayos. Se detallan métodos para determinar el ácido ascórbico en una tableta de vitamina C y en pimientos utilizando titulación de yodato de potasio, voltamperometría y espectrofotometría. El objetivo es medir la cantidad de vitamina C presente y verificar que cumple con los estándares de calidad requeridos.