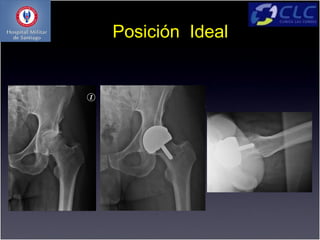
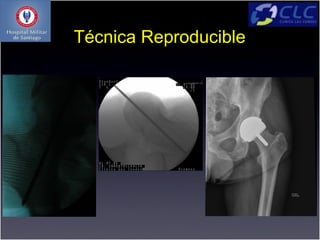
Este documento describe la técnica quirúrgica de resurfacing de cadera. Ofrece una filosofía conservadora al reemplazar solo la superficie dañada en lugar de resecar la cabeza y el cuello femoral. Proporciona las características, ventajas y desventajas de esta técnica, así como la experiencia de varios autores. Finalmente, resume la experiencia del autor con 76 casos de resurfacing de cadera.