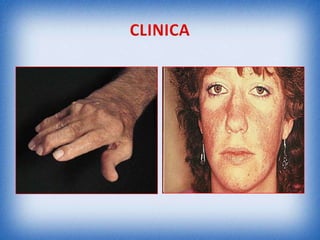
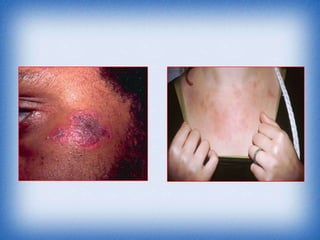
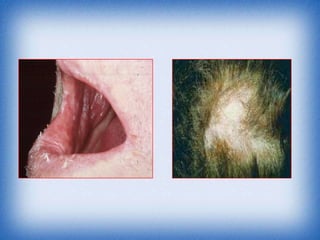
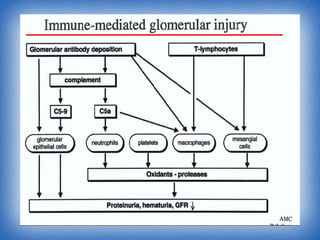
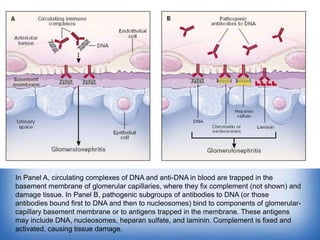
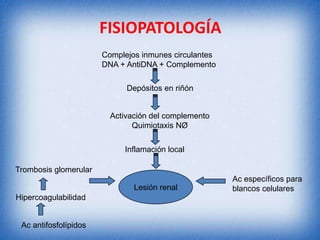
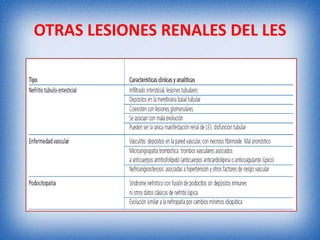
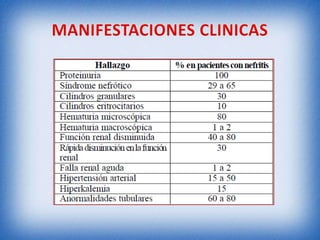
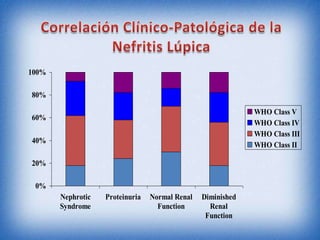
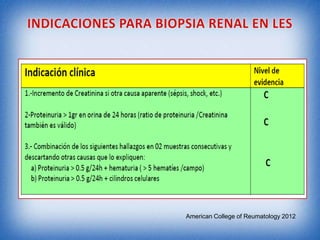
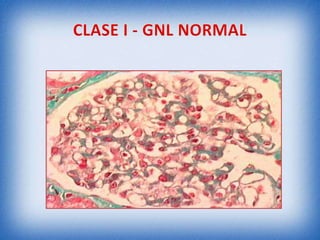
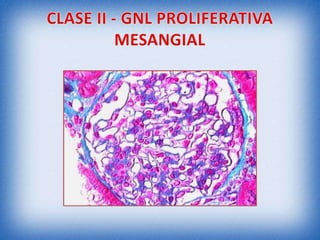
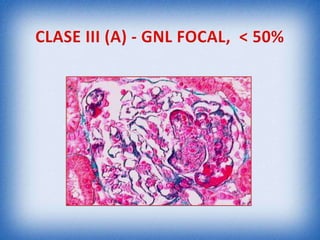
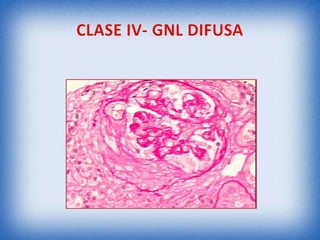
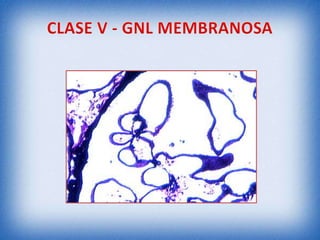
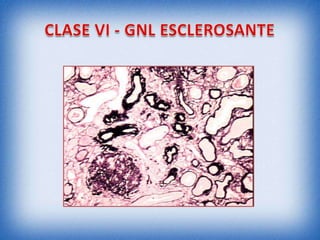
La nefritis lúpica es la afectación renal más común en el lupus eritematoso sistémico. Afecta principalmente a mujeres latinas y afroamericanas entre 16-55 años. El diagnóstico se realiza mediante biopsia renal que muestra depósitos de complejos inmunes que activan el complemento y causan inflamación y daño renal. El tratamiento incluye corticoides e inmunosupresores con el objetivo de lograr remisión renal y prevenir recaídas y enfermedad renal en etapa terminal.