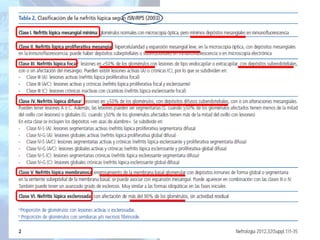
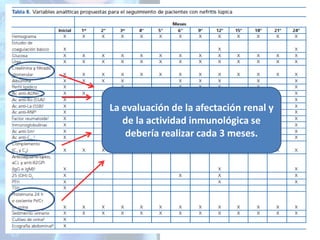
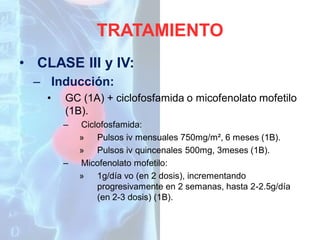
Este documento presenta el caso clínico de una mujer de 49 años diagnosticada con nefritis lúpica. Describe su historia clínica, incluyendo síntomas iniciales de poliartritis, diagnóstico de LES, y más recientemente edemas y proteinuria indicativos de afectación renal. Se realizó una biopsia renal que confirmó el diagnóstico de nefritis lúpica proliferativa. El documento revisa las pautas generales para el tratamiento de la nefritis lúpica, incluyendo el uso de corticoides, hid