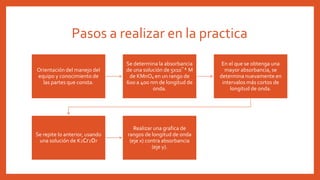
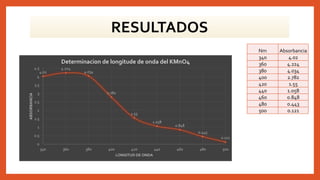
En esta práctica de laboratorio se determinó la longitud de onda de máxima absorción de iones permanganato y dicromato usando un espectrofotómetro. Se midió la absorbancia de una solución de KMnO4 en un rango de longitudes de onda y se encontró que la absorción máxima ocurría entre 340-360 nm. Luego, se repitió el procedimiento para una solución de K2Cr2O7 y se graficaron los resultados para mostrar cómo variaba la absorbancia con la longitud de onda.