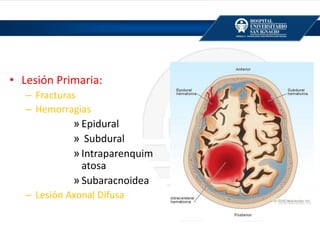
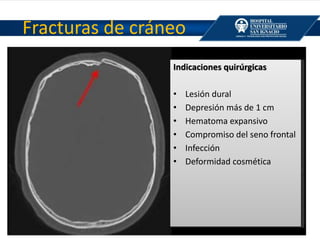
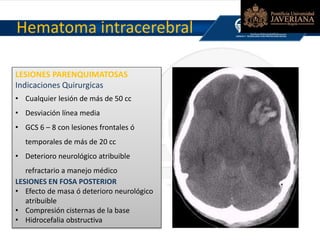
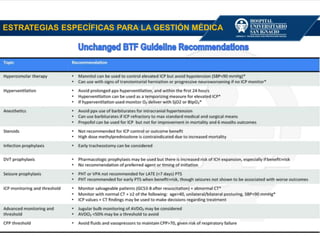
El documento aborda la epidemiología y mortalidad relacionadas con lesiones cerebrales traumáticas (TCE), destacando que 1.7 millones de estadounidenses sufren estas lesiones anualmente, con alta incidencia en varones jóvenes y un aumento en mortalidad asociado al consumo de alcohol. Se describen los mecanismos de trauma, clasificaciones de TCE y las indicaciones quirúrgicas para diferentes tipos de hematomas, además de incluir datos sobre manejo médico, monitorización neurológica, y estrategias neuroprotectoras y de manejo en la sala de emergencias. La información es relevante para la práctica médica en el manejo de TCE en urgencias y cuidados críticos.