Abordaje urgente de la compresión medular oncológica
- 1. Abordaje de la compresión medular desde el servicio de urgencias. Sara Giner Ruiz C.S Rebolería Jorge Guilermo Pérez Castán C.S. Almozara
- 2. ÍNDICE Introducción Anamnesis Clínica Diagnóstico Diagnóstico diferencial Pruebas complementarias Tratamiento Derivación de pacientes con síntomas de compresión medular de origen tumoral. Bibliografía
- 3. Introducción La compresión medular (CM) o de cauda equina está provocada por compresión directa y/o inducción de colapso vertebral o inestabilidad por diseminación metastásica o extensión directa de una tumoración que amenaza con provocar discapacidad neurológica Según el NHS la incidencia en países como Escocia o Canadá se sitúa en 80 casos por millón de habitantes/año (4000 casos al año en el Reino Unido) por lo que en nuestra Comunidad, siendo la población, según el último censo del año 2011, de 1.314.906, atenderíamos unos 105 pacientes al año. Además, el 50-70% de los pacientes con cáncer presentan evidencia de enfermedad metastásica en el momento del éxitus. La compresión medular oncológica es la segunda complicación más frecuente en el paciente con cáncer tras la metástasis cerebral. Se trata de una emergencia médica ya que el diagnóstico y el tratamiento precoz son indispensables para lograr efectividad terapéutica y evitar efectos neurológicos como la pérdida del control de esfínteres o parálisis irreversible, lo cual tiene un gran impacto en la morbimortalidad del paciente. Se da en un 5% de pacientes oncológicos y el origen más frecuente es el cáncer de pulmón, próstata y mama representando hasta un 60% de los casos. Asimismo, la CM es la forma de presentación inicial de hasta un 20% de tumores siendo la mayoría de ellos de origen pulmonar, mielomas, TOD y LNH. En el 75% de los casos el origen de la CM es el colapso vertebral por una metástasis del cuerpo vertebral por vía hematógena. El lugar más frecuente de aparición es la columna torácica (60%), en segundo lugar la lumbosacra (30%) y por último, la cervical (10%). Aunque entre 10-38% de los pacientes habrá más de un nivel afecto. Clínica El dolor es el síntoma más frecuente y aparece en el 80-95% de los pacientes. Suele ser progresivo, localizado a nivel de la lesión y de características puramente mecánicas. Cuando existe afectación de raíces nerviosas o de la cola de caballo el dolor suele ser radicular uni o bilateral. La claudicación es el segundo síntoma más frecuente (61-89%) y generalmente aparece de forma gradual y de predominio en musculatura proximal, aunque progresivamente se afectará también la musculatura distal, lo que comprometerá la deambulación. Las alteraciones de la sensibilidad se presentan en un 46-80% de los pacientes. Son parestesias e hipoestesias que se inician distalmente y van ascendiendo hasta el nivel de la afectación. En caso de afectación de la cola de caballo, la pérdida de sensibilidad se localiza en región perineal y en región medial de ambas piernas. Sin embargo, no todas las metástasis espinales van a provocar déficit neurológico. La compresión epidural-medular ocurre en: - Un 5-10% de los pacientes con cáncer. - Hasta en un 40% de los pacientes con lesiones óseas metastásicas. Existen estudios que correlacionan el riesgo de sufrir déficits neurológicos en dependencia del órgano en el cual asienta el tumor primario, así la incidencia de dichos déficits en el caso del cáncer de mama es del 22%, pulmón 15% y próstata 10%.
- 4. La velocidad de instauración de los síntomas marca la gravedad de la urgencia y es inversamente proporcional a la probabilidad de reversibilidad del cuadro, siendo reversible si la clínica se ha iniciado hace menos de 24-48 horas. Diagnóstico Una cuidadosa anamnesis y una exploración física completa deben ser el primer paso ante un paciente con sospecha clínica de compresión medular. Se deben evaluar todos los grupos musculares y hacer un estudio de las sensibilidades, valorando si existe un nivel sensitivo, lo que permitirá localizar los estudios de neuroimagen necesarios. Se recomienda realizar una exploración detallada siguiendo el esquema ASIA (Anexo 1), definiendo la lesión medular en la escala ASIA A-E. La atención inicial ante un paciente que acude al servicio de urgencias con sospecha de compresión medular la realizará el personal médico del Servicio de Urgencias. Una vez confirmada la sospecha clínica, se recomienda consultar con el Servicio de Neurología. En caso de antecedente oncológico, el neurólogo consultará con el Servicio de Oncología. Se considera que si existe una lesión completa ASIA A clínicamente documentada de más de 72 horas de evolución el cuadro es irreversible, pudiéndose realizar el diagnóstico etiológico de forma programada.
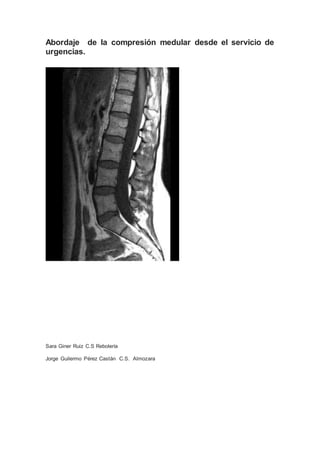
- 5. En cuanto al diagnóstico diferencial, en pacientes oncológicos existen distintas causas de disfunción de la médula espinal: 1. Compresión medular cuyas causas pueden ser un tumor, absceso, hematoma, hernia discal o hemangioma vertebral. 2. Proceso intramedular producido por la presencia de metástasis, absceso, hematoma o siringomielia. 3. Mielopatía tras tratamiento con radioterapia o quimioterapia intratecal, por un proceso paraneoplásico… 4. Metástasis Leptomeníngea 5. Aracnoiditis Pruebas complementarias Una buena historia clínica nos ayudará a enfocar el cuadro clínico así como a orientar el nivel de la afectación, aunque la confirmación del diagnóstico se basa en pruebas de imagen. La radiografía de columna pese a usarse como prueba inicial, tiene una baja especificidad por lo que cuenta con una elevada tasa de falsos negativos. La gammagrafía ósea es más sensible que la radiografía simple pero menos especifica. No se usa en situaciones de urgencia. La RMN es la herramienta considerada como gold standard. Posee una sensibilidad del 93% y una especificidad del 97%.
- 6. Las secuencias empleadas son T1 y T2. En T1 el tumor es hipointenso en relación con la médula espinal normal, a diferencia de los niveles irradiados previamente que mostrarán hiperintensidad. En cambio en T2 el tumor mostrará una señal hiperintensa. El uso de gadolinio permitirá una mejor valoración del espacio epidural y tener más precisión para discernir entre masas paravertebrales y metástasis extramedulares intradurales, intramedulares o leptomeníngeas. La RMN debe realizarse en las primeras 24 h tras el inicio de la clínica. Existe una escala que nos permitirá clasificar las compresiones así como la elección de la técnica terapeútica. Grado 0 – Tumor confinado al hueso. Grado 1 – Tumor con extensión epidural sin contacto con la médula espinal o impronta en la médula espinal sin desplazamiento. Grado 2 – Tumor que desplaza o comprime el cordón medular sin extensión circunferencial de tumor u obliteración del espacio del del LCR. Grado 3 – Tumor con extensión circunferencial epidural y/o tumor que causa compresión medular grave con obliteración del espacio del del LCR. Se consideran de bajo grado las imágenes radiológicas grado 1 y de alto grado las imágenes radiológicas grados 2 y 3. Se recomienda realizar RMN de toda la columna porque hasta en 1/3 de los pacientes presentan enfermedad en varios niveles, lo cual afecta tanto al tratamiento como al pronóstico y porque el nivel de afectación clínica puede no corresponderse con la localización de la CM. Resulta de especial relevancia el saber discernir el momento en el que se debe realizar dicha prueba de imagen para comenzar con una actitud precoz y así obtener mejor pronóstico. En pacientes con clínica de compresión medular o síndrome de cola de caballo de aparición aguda e inesperada, es decir, no de causa tumoral, se realizará RM espinal de urgencia a ser posible en las primeras 6 horas. En estos casos surge el obstáculo de la situación clínica del paciente, ya que la resonancia magnética es una prueba de larga duración y si el paciente se encuentra con mucho dolor no podrá aguantar la realización de todas las secuencias por lo que es en este caso cuando el radiólogo decidirá qué secuencias obtener en el menor tiempo posible. Si se trata de pacientes con sospecha clínica de compresión medular y sintomatología progresiva en días se realizará la exploración de RM espinal en el plazo de 24 horas. En pacientes con síntomas neurológicos estables de semanas de evolución, incluso meses, el estudio de RM espinal será realizado en plazo menor a una semana, preferentemente entre 3-5 días. Si dicha prueba de imagen no está disponible o las características del paciente no permiten su realización como se ha mencionado anteriormente, se realizará TC urgente. Al ser la mayoría de los pacientes de tipo oncológico, es plausible que nos encontremos con que dispongan de un estudio radiológico reciente mediante TC por lo que en estos casos será factible revisar minuciosamente las imágenes en un segundo tiempo de forma que se pueda demostrar ausencia de invasión del canal medular estableciendo un diagnóstico de confianza que excluya la necesidad de la exploración de RM a corto plazo. En caso de existir invasión del canal medular, independientemente de que presente o no clínica, se deberá realizar una resonancia en un plazo máximo de 1 a 2 semanas.
- 7. En caso de solicitud de RM urgente, es necesario comentar el caso clínico con el neurorradiólogo de guardia, para programar el estudio de RM. Si la clínica del paciente oncológico es exclusivamente dolor, sin presentar focalidad neurológica, y siendo el resto de pruebas complementarias normales, la exploración de RM puede hacerse de forma preferente en 1 mes aproximadamente. En caso de rápida progresión de la sintomatología se deberá realizar según los apartados anteriores, comentando el caso con el Servicio de Neurorradiología. En cuanto a esta última prueba diagnóstica, el TC, tiene menor sensibilidad y especificidad por lo que resulta más difícil distinguir el espacio epidural y el cordón medular. La escala de inestabilidad espinal SINS clasifica a las CM oncológicas de la siguiente manera: score 0-6: estabilidad; score 7-12: potencialmente inestable; score 13-18: inestable. Es necesario garantizar la existencia de estabilidad antes de iniciar RT.
- 8. Diagnóstico etiológico Sólo es necesario en aquellos pacientes sin antecedentes de cáncer o que han permanecido libres de enfermedad durante un largo periodo de tiempo. En estos casos realizar una biopsia por vía quirúrgica nos aporta además del diagnóstico histológico la posibilidad de resolver el problema compresivo. Planificación de ingreso Una vez hallado el problema del paciente y haber sido constatado mediante pruebas de imagen, hemos de saber cómo y cuándo actuar. Si el paciente va a ser intervenido quirúrgicamente de forma urgente el paciente deberá de ser ingresado en el Servicio de Neurocirugía. No obstante, si el paciente no tiene antecedente oncológico será ingresado en el Servicio de Neurología para posterior estudio y si tiene antecedente oncológico posiblemente relacionado con el evento actual, será ingresado en el Servicio de Oncología. También puede darse el caso de que el paciente ya disponga de una e lesión medular establecida por lo que en esta ocasión se contactará con Unidad de lesionados medulares (ULME) para iniciar programa de tratamiento integral e individualizado de manera oportuna y el paciente ingresara en la ULME si es candidato a tratamiento neurorrehabilitador. Tratamiento Los objetivos del tratamiento son aliviar el dolor, preservar o mejorar la función neurológica, estabilizar la columna, el control local del tumor y mejorar la calidad de vida. Existen varias opciones terapéuticas que se pueden aplicar solas o combinadas, pero antes debemos valorar siempre: 1. Situación neurológica del paciente. 2. Radiosensibilidad del tumor. 3. Estabilidad mecánica: dolor con el movimiento. 4. Extensión de la enfermedad y situación clínica del paciente. La efectividad del tratamiento va a depender de la velocidad de instauración de los síntomas y del estado previo del paciente, siendo un factor pronóstico muy importante la conservación de la capacidad de deambulación. Un lento desarrollo se relaciona con una mejor evolución. Como medidas y cuidados generales se recomienda colocar Sonda Vesical Permanente, (SVP), de material siliconado, sonda Nasogástrica, (SNG), en pacientes afectos de íleo paralítico. Si se prevee que el paciente no se podrá trasladar en las primeras horas, se iniciará tratamiento profiláctico de Trombosis Venosa Profunda, con Heparina de Bajo Peso Molecular, subcutánea cada 24 horas a dosis profiláctica según peso del paciente, dieta absoluta y protección gástrica. Añadido a lo anteriormente descrito, se deberán realizar movilizaciones en bloque hasta que el facultativo responsable indique lo contrario. Igualmente se deberán realizar prevención de las úlceras por decúbito con cambios posturales y planos de almohadas por parte de enfermería y personal auxiliar.
- 9. En primer lugar, se ha de abordar el tratamiento sintomático, por lo general los pacientes presentan dolor de muy elevada intensidad y de difícil control por la destrucción vertebral que puede verse acompañada de fracturas patológicas o inestabilidad mecánica segmentaria por lo que la primera actuación es la administración de analgesia mediante antiinflamatorios no esteroideos (AINES) y/o con opiodes. Corticoide En pacientes con dolor y déficit neurológico asociado es el tratamiento inicial. Deben pautarse precozmente, ante la sospecha clínica de SCM puesto que disminuyen el edema vasogénico mejorando el dolor relacionado con el tumor en un 60% de los casos, por lo que se ha visto que el beneficio es inmediato. No hay consenso en la dosis inicial de dexametasona a administrar, ya que dosis altas (100 mg-40 mg/día) no han demostrado mayor eficacia que dosis más bajas (32-16 mg/día) en cuanto a la disminución del dolor y al porcentaje de pacientes deambulantes posttratamiento. Las dosis que se suelen utilizar son de 100 mg en infusión continua durante 30 minutos, seguidas de 16 mg/6 h durante 2 días y, posteriormente, pauta descendente de 4 mg cada 2 días. En los pacientes sin disfunción neurológica, sólo con dolor, con invasión del canal medular inferior al 50% y con afección de un máximo de 2 zonas vertebrales, no sería necesario iniciar tratamiento con dexametasona, ya que se observan excelentes resultados c on radioterapia exclusiva. Se recomienda usar inhibidores de la bomba de protones (IBP) a dosis altas cuando se inicia tratamiento con corticoides. (Omeprazol 40 iv / 24h). En pacientes con inestabilidad mecánica, así como en histologías radiorresistentes o en aquellos que presenten empeoramiento durante el tratamiento de radioterapia se opta por la cirugía, siempre que no existan contraindicaciones quirúrgicas.
- 10. Radioterapia La RT es un pilar fundamental en el tratamiento de la CM. Es el tratamiento de elección en aquellos pacientes con contraindicaciones quirúrgicas y en aquellos con estabilidad de la columna vertebral que presenten disfunción neurológica y dolor. Numerosos estudios aleatorizados analizan la opción de radioterapia con y sin corticoides resultando más beneficiosa la asociación. En 60-90% de los pacientes la combinación de corticoide+ RT conseguirá aliviar el dolor. No debe administrarse de modo preventivo, en pacientes con metástasis vertebrales asintomáticos. Es importante tener en cuenta que al desaparecer el tejido tumoral, se favorece el colapso vertebral por lo que de manera preventiva, los pacientes con lesiones en estas áreas, se benefician de llevar un sistema ortopédico de refuerzo que favorece la sujeción, como los corsés ortopédicos. Los tumores radiosensibles y por lo tanto que mejor responderán a la RT son linfomas, mielomas, cáncer de pulmón de células pequeñas, tumor de células germinales, cáncer de próstata, cáncer de mama y de ovario. Por contraposición, los melanomas, los tumores de origen renal, el cáncer de pulmón no microcítico, los tumores gastrointestinales y los sarcomas se consideran histologías radiorresistentes. La dosis y el fraccionamiento dependerá de la histología del tumor así como del performance status y de la esperanza de vida del paciente, optando por esquemas más largos (30-40 Gy en 10-20 fracciones) en caso de pacientes con larga esperanza de vida porque mejoran el control a largo plazo y suelen asociarse a mejor riesgo de recaídas y por esquemas de ciclos cortos (20 Gy en 5 fracciones) o incluso una sesión única (8 Gy) en pacientes con esperanza de vida inferior a 6 meses, ya que los ciclos más largos no han demostrado superioridad. En un metaanálisis reciente de 2019 de Donovan et al comparan la fracción única frente a los ciclos cortos en pacientes con escasa esperanza de vida sin haber encontrado diferencias en la respuesta motora, disfunción vesical o supervivencia global tras RT. El campo de radiación es un cuerpo vertebral por encima o otro por debajo de la metástasis epidural. En caso de que existiese columna estable o si se hubiese dado RT previa sobre la zona se podría valorar la realización de SBRT. En aquellos pacientes en los que exista afectación en varios niveles se tratarán sólo los que producen sintomatología.
- 11. Cirugía De forma general se podrían indicar cirugía en los siguientes supuestos: 1. Compresión en un nivel irradiado previamente o progresión en curso de radioterapia. 2. Clínica rápidamente progresiva sin confirmación histológica (en el acto quirúrgico se recogerá material histológico para el diagnóstico y posterior tratamiento oncológico con radioterapia y/o quimioterapia y/o hormonoterapia) 3. Columna inestable o fractura patológica. 4. Tumores radiorresistentes, deben valorarse de modo aislado, en función de la indicación más adecuada a cada caso. Quimioterapia El tratamiento con quimioterapia se deberá considerar en todos pacientes, en los que haya sido obtenido el diagnostico histológico, y presenten tumores quimiosensibles. Complicaciones del tratamietno TVP y TEP: compresión neumática intermitente además de medias elásticas (Clase I, Nivel B) a aquellos pacientes que se encuentren encamados con compresión medular. Se puede plantear el inicio de heparina subcutánea de bajo peso molecular para prevenir tromboembolismos, en aquellos pacientes con ausencia de movilidad tras 1 a 4 días del inicio del cuadro, una vez se haya descartado sangrado activo (Clase IIb, Nivel B). Pronóstico y funcionalidad La supervivencia a corto plazo y la esperanza de vida global de las personas con LM han mejorado de forma espectacular a lo largo de los últimos 30 años. Sin embargo, la esperanza de vida de los lesionados medulares sigue siendo inferior a la de la población general. Las primeras causas de muerte son cardiopatía (19%); causas externas como accidentes, suicidio y violencia (18%); neumopatía, especialmente neumonía (18%), y septicemia (10%)28. La muerte por suicidio es aproximadamente cinco veces más frecuente en personas con LM que en la población general y representa aproximadamente el 9% de las muertes. La mayoría de los suicidios se producen los primeros 5 años después de la lesión. En el pronóstico de la LM el factor más relevante es la valoración neurológica según la clasificación ASIA. El examen neurológico que sirve como base para predecir la evolución neurológica es el realizado a las 72 horas del inicio del tratamiento específico. Esta exploración inicial sirve no sólo para establecer el pronóstico, sino también para detectar deterioro en el estado neurológico del paciente.
- 12. En los pacientes con lesiones medulares incompletas, el 50-66% de la recuperación motora en el primer año ocurre en los dos primeros meses después de la lesión; la recuperación continúa, pero es más lenta después de 3-6 meses; además se ha comprobado recuperación motora hasta dos años post-lesión. Basándonos en la valoración neurológica en la primera semana de evolución, el 90% de pacientes con lesión completa (ASIA A) siguen con LM completa; de los que se convierten en LM incompleta, el 3% recuperarán fuerza funcional en los miembros inferiores. En el caso de los pacientes inicialmente clasificados como ASIA B, aproximadamente el 50% realizarán marcha si la preservación sensitiva es para el dolor (síndrome posterior); pero si sólo lo es para el tacto (síndrome anterior), llegarán a deambular el 10-30%. La mayoría de pacientes con lesión incompleta motora recuperan la capacidad de marcha. Alrededor de un 75% de los individuos con lesiones ASIA C realizan “marcha comunitaria”. El pronóstico resulta excelente para aquellos inicialmente clasificados como ASIA D. En lesiones incompletas la edad supone un factor pronóstico muy importante; el pronóstico funcional es peor en los mayores de 50 años. Con frecuencia los pacientes con lesión medular cervical completa recuperan un nivel funcional en la zona proximal de la lesión (recuperación de la raíz). Los estudios se han centrado en la recuperación de los músculos con un balance muscular menor de tres, localizados por debajo del nivel lesional. De los músculos infralesionales con algún balance muscular inicial (grados 1/5 ó 2/5), el 90% recuperan fuerza contra gravedad al año. Actualmente, gracias al progreso de la Medicina, la morbi-mortalidad 2ª a LM ha descendido drásticamente. Ha habido, por tanto, un aumento considerable de la expectativa de
- 13. vida en los lesionados medulares. Este incremento de la expectativa de vida amplía el campo de actuación y los retos que se plantean en la atención de estos pacientes. Existen unas tablas de recuperación funcional esperada en función del nivel lesional, si bien en función de diversos factores como la morbilidad del paciente, dicha recuperación puede ser diferente.
- 14. DERIVACIÓN DE PACIENTES CON SINTOMAS DE COMPRESION MEDULAR DE ORIGEN TUMORAL. Existe una particularidad en la organización de las guardias de Neurocirugía en la Comunidad de Aragón, de tal forma que los dos servicios existentes se alternan el turno de guardia semanalmente para urgencias externas. Así pues, una semana está de guardia el Servicio de Neurocirugía del Hospital Universitario Miguel Servet y la siguiente semana está de guardia el Servicio de Neurocirugía del Hospital Universitario Lozano Blesa. Se deberá contactar previamente con el Servicio de Neurocirugía que esté de guardia, para valorar si procede el traslado. Se deberá realizar en el hospital de procedencia el estudio más completo posible (TC y RM si se dispone) para poder realizar una correcta valoración previa al traslado. Bibliografía 1. Robson P. Metastatic spinal cord compression: a rare but important complication of Clin Med (Lond). 2014 Oct;14(5):542-5. doi: 10.7861/clinmedicine.14-5-542. PMID: 25301920; PMCID: PMC4951968. 2. Cole JS, Patchell RA. Metastatic epidural spinal cord compression. Lancet Neurol. 2008 May;7(5):459-66. doi: 10.1016/S1474-4422(08)70089-9. PMID: 3. Abu-Ghanem S, Sidon E, Shemesh S, Amital A, Ohana [Metastatic spinal cord compression: diagnosis and treatment]. Harefuah. 2013 Dec;152(12):720-4, 752. Hebrew. PMID: 24482996. 4. Patel DA, Campian JL. Diagnostic and Therapeutic Strategies for Patients with Malignant Epidural Spinal Cord Compression. Curr Treat Options Oncol. 2017 Aug 10;18(9):53. doi: 10.1007/s11864-017-0497-6. PMID: 28795286. 5. Bilsky MH, Laufer I, Fourney DR, et al. Análisis de confiabilidad de la escala de compresión de la médula espinal epidural. J Neurosurg Spine 2010; 13: 6. Fisher CG, DiPaola CP, Ryken TC, Bilsky MH, Shaffrey CI, Berven SH, Harrop JS, Fehlings MG, Boriani S, Chou D, Schmidt MH, Polly DW, Biagini R, Burch S, Dekutoski MB, Ganju A, Gerszten PC, Gokaslan ZL, Groff MW, Liebsch NJ, Mendel E, Okuno SH, Patel S, Rhines LD, Rose PS, Sciubba DM, Sundaresan N, Tomita K, Varga PP, Vialle LR, Vrionis FD, Yamada Y, Fourney DR. A novel classification system for spinal instability in neoplastic disease: an evidence-based approach and expert consensus from the Spine Oncology Study Spine (Phila Pa 1976). 2010 Oct 15;35(22):E1221-9. doi: 10.1097/BRS.0b013e3181e16ae2. PMID: 20562730. 7. Sørensen S, Helweg-Larsen S, Mouridsen H, Hansen Effect of high-dose dexamethasone in carcinomatous metastatic spinal cord compression treated with radiotherapy: a randomised trial. Eur J Cancer. 1994;30A(1):22-7. doi: 10.1016/s0959- 8049(05)80011-5. PMID: 8142159. 8. Shiloh R, Krishnan Radiation for Treatment of Painful Bone Metastases. Hematol Oncol Clin North Am. 2018 Jun;32(3):459-468. doi: 10.1016/j.hoc.2018.01.008. Epub 2018 Mar 17. PMID: 29729781. 9. Bernier J, Hall EJ, Giaccia Radiation oncology: a century of achievements. Nat Rev Cancer. 2004 Sep;4(9):737-47. doi: 10.1038/nrc1451. PMID: 15343280. 10. Abuzallouf Spinal cord compression, an overview for radiation oncologists. Gulf J Oncolog. 2007 Jul;(2):29-32. PMID: 20084721. 11. Donovan EK, Sienna J, Mitera G, Kumar-Tyagi N, Parpia S, Swaminath Single versus multifraction radiotherapy for spinal cord compression: A systematic review and meta- analysis. Radiother Oncol. 2019 May;134:55-66. doi: 10.1016/j.radonc.2019.01.019. Epub 2019 Feb 2. PMID: 31005225. 12. Tree AC, Khoo VS, Eeles RA, Ahmed M, Dearnaley DP, Hawkins MA, Huddart RA, Nutting CM, Ostler PJ, van As NJ. Stereotactic body radiotherapy for oligometastases. Lancet Oncol. 2013 Jan;14(1):e28-37. doi: 10.1016/S1470-2045(12)70510-7. 13. Protocolo Hospital Universitario Miguel Servet 2021
- 15. 14. Harrington KD: Metastatic tumors of the spine: diagnosis and treatment. J Am Acad Orthop Surg 1:76–86, 1993. 15. Bohm P, Huber J: The surgical treatment of bony metastases of the spine and limbs. J Bone Joint Surg Br 84:521–529, 2002. 16. Wong DA, Fornasier VL, MacNab I: Spinal metastases: the obvious, the occult, and the impostors. Spine 15:1–4, 1990. 17. Sundaresan N, Digiacinto GV, Hughes JE, Cafferty M, Vallejo A. 18. Treatment of neoplastic spinal cord compression: results of a prospective study. Neurosurgery 29: 645-650, 1991.
