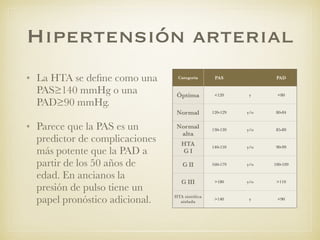
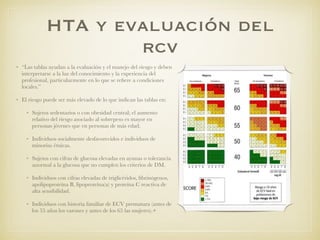
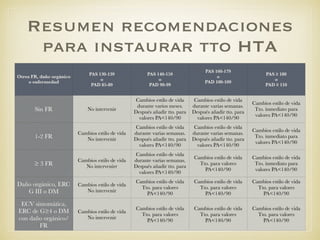
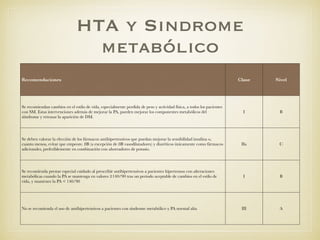
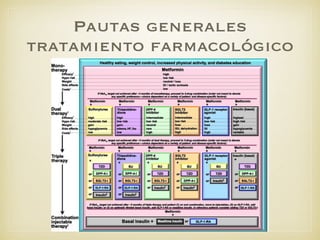
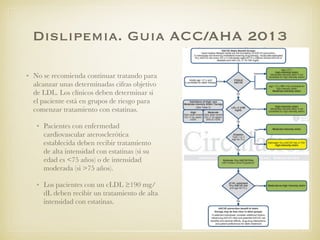
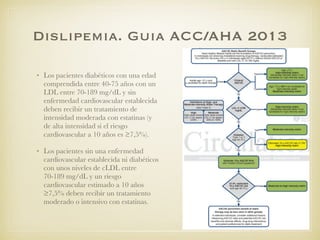
El documento define el síndrome metabólico y sus componentes, incluyendo obesidad central, hipertrigliceridemia, bajos niveles de HDL, hipertensión y hiperglucemia. Explica que la prevalencia del síndrome metabólico está aumentando debido al incremento de la obesidad a nivel mundial y analiza factores de riesgo como la genética, resistencia a la insulina, dislipemia e hipertensión. Finalmente, discute la asociación entre el síndrome metabólico y un mayor riesgo