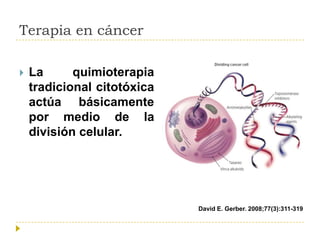
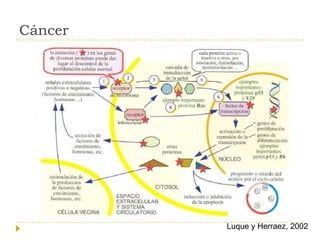
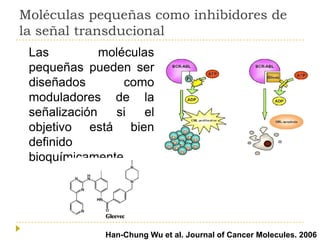
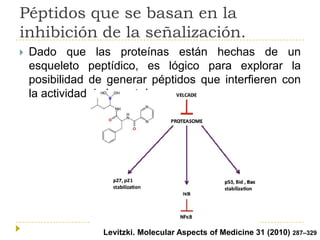
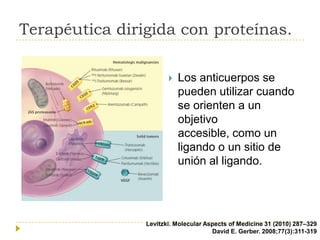
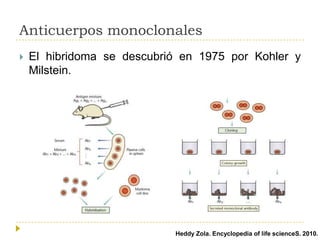
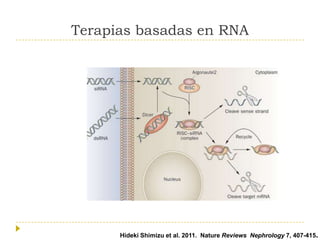
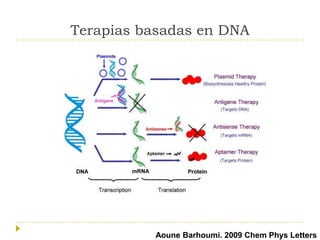
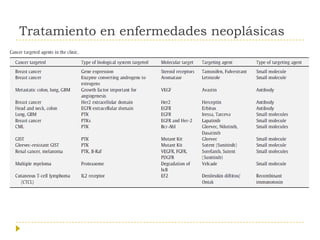
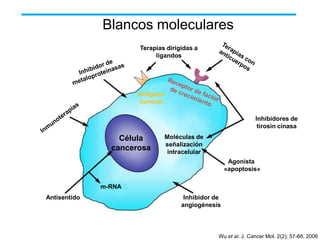
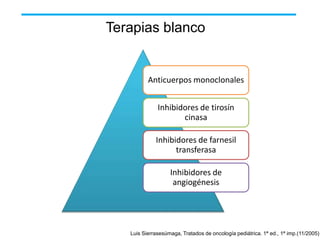
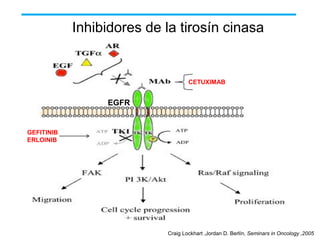
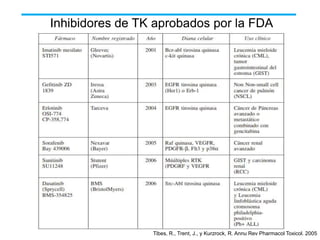
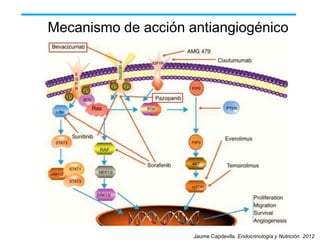
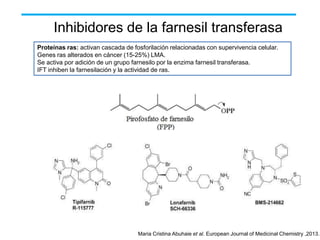
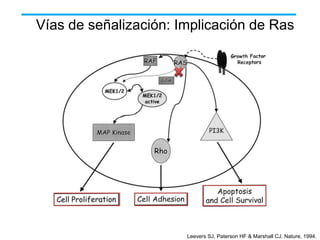
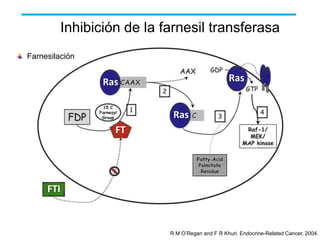
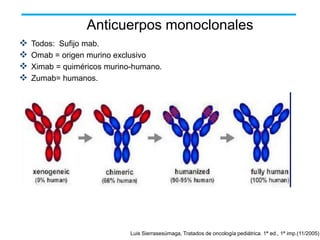
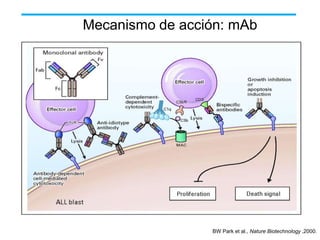
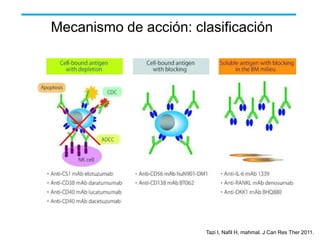
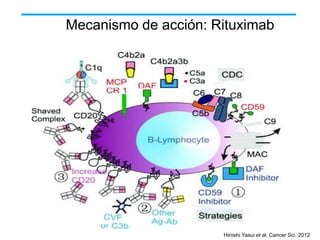
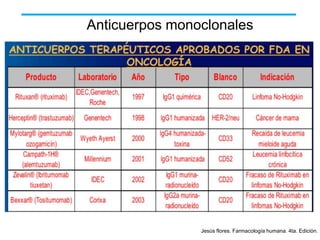
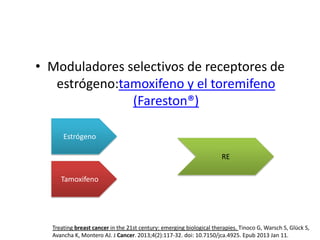
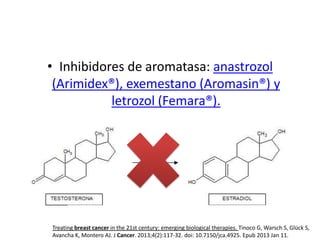
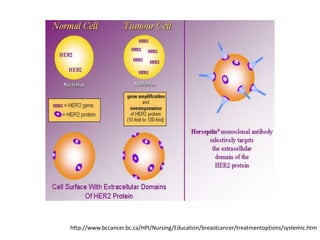
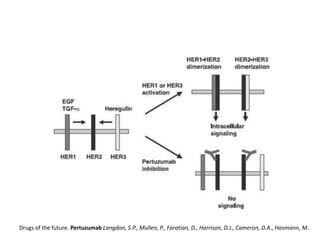
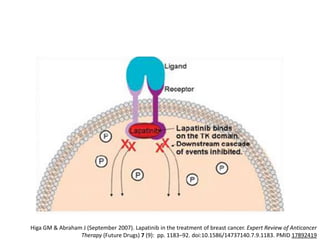
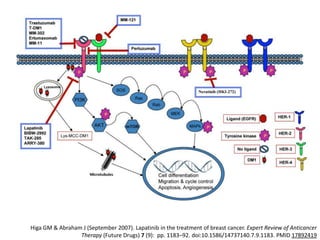
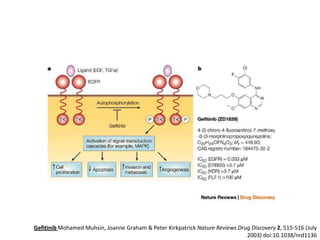
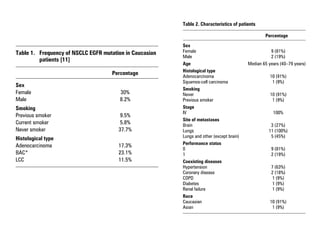
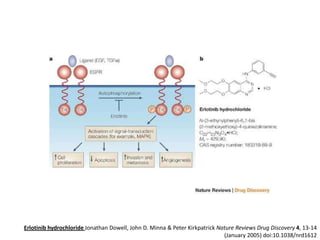
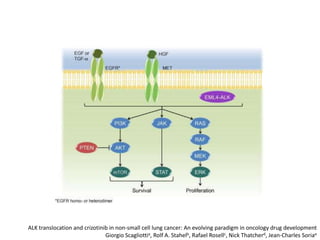
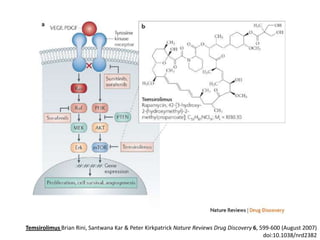
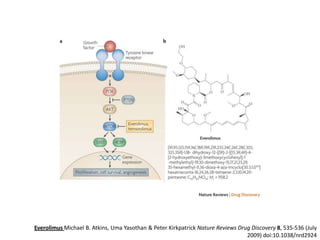
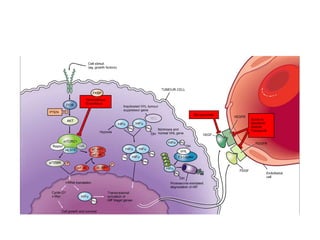
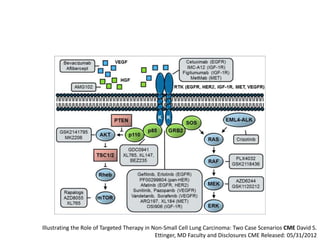
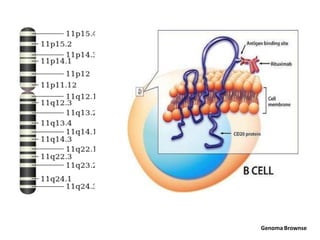
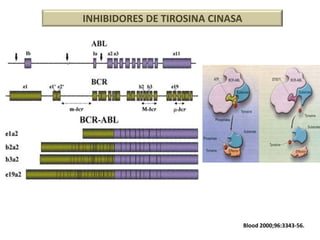
El documento describe varios tipos de terapias dirigidas utilizadas en el tratamiento del cáncer. Estas terapias incluyen moléculas pequeñas como inhibidores de señalización, péptidos que inhiben la señalización, terapia dirigida con proteínas como anticuerpos monoclonales, y nanopartículas para la liberación de medicamentos. Se mencionan varios blancos moleculares específicos y fármacos aprobados para el tratamiento de cánceres como mama, pulmón y páncre