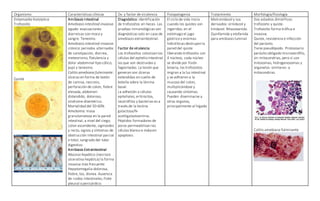
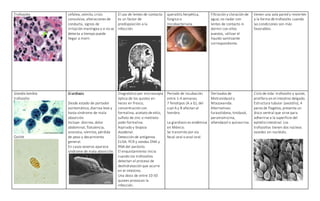
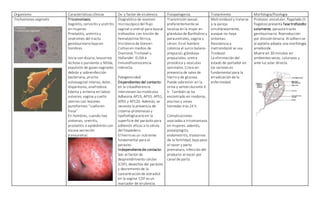
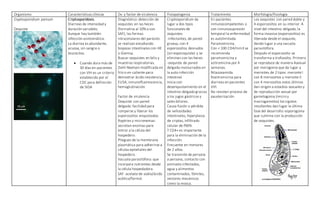
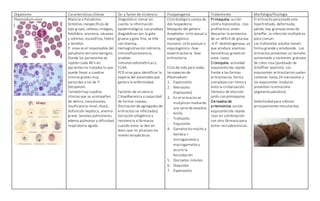
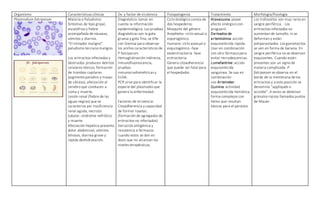
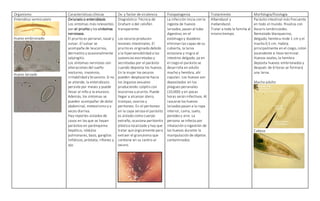
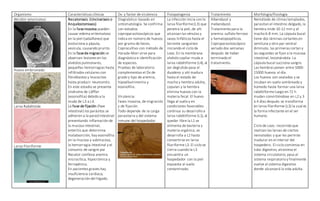
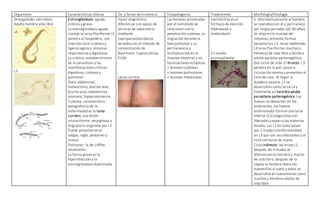
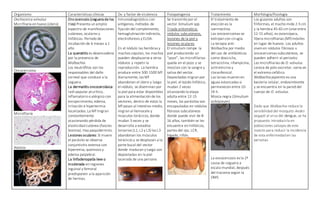
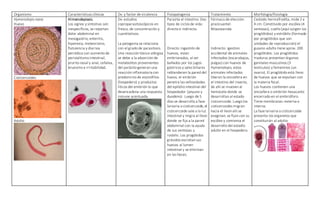
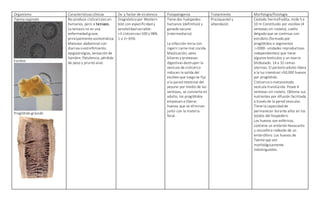
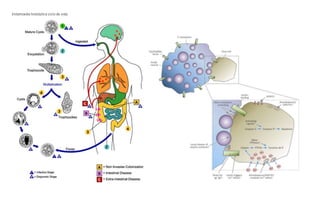
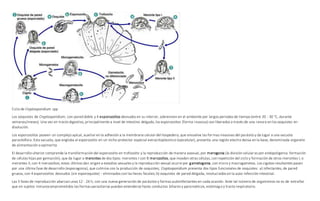
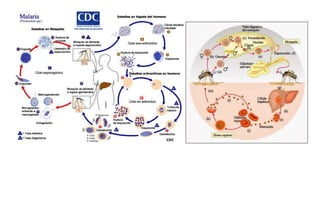
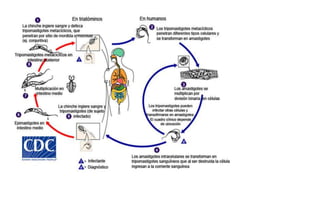
El documento describe las características de varios organismos protozoarios parásitos del tracto gastrointestinal y genitourinario humano. Entre ellos se encuentran Entamoeba histolytica, la cual causa amibiasis intestinal y extraintestinal, incluyendo abscesos hepáticos. También se mencionan Naegleria fowleri y Acanthamoeba gruberi, los cuales pueden causar meningoencefalitis. Otro parásito descrito es Giardia lamblia, que provoca giardiasis. Finalmente, se detalla a Cryptospor