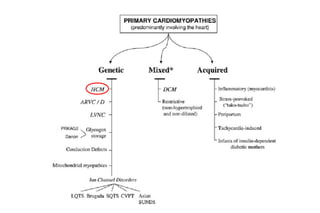
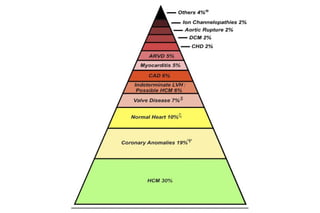
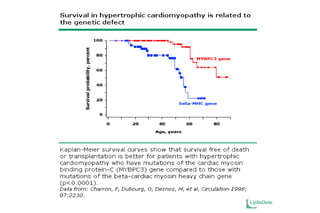
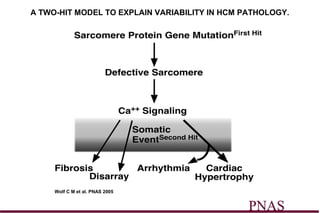
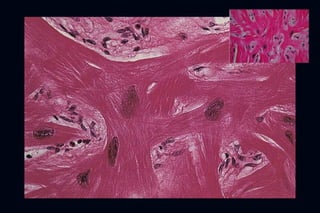
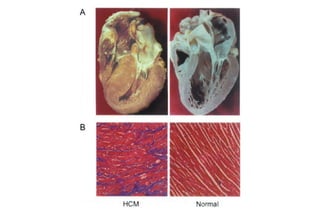
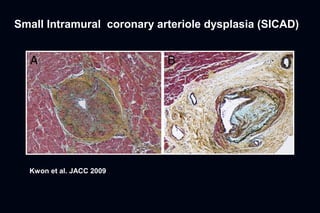
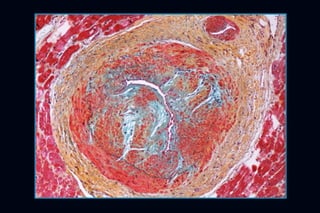
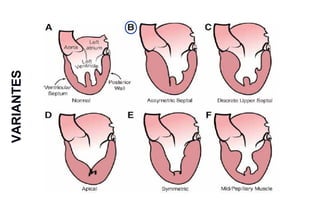
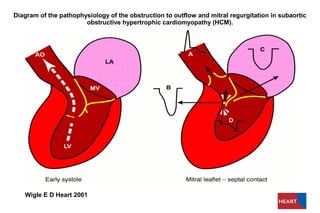
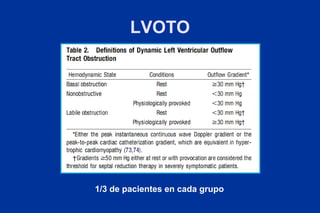
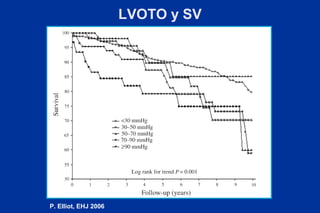
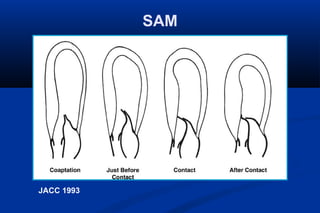
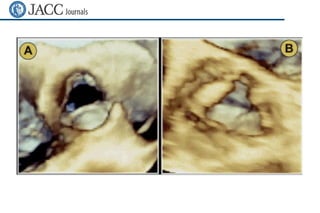
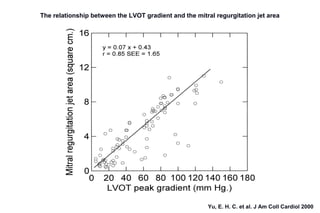
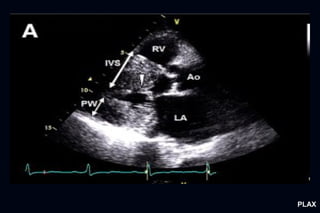
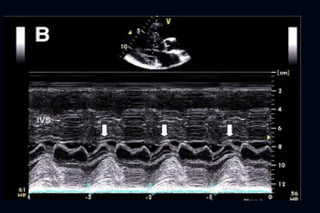
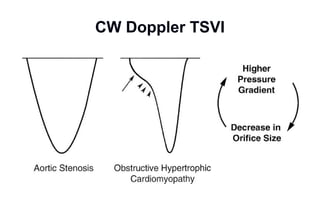
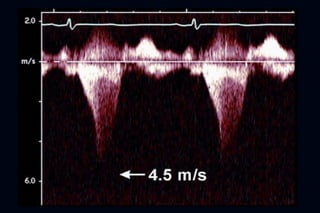
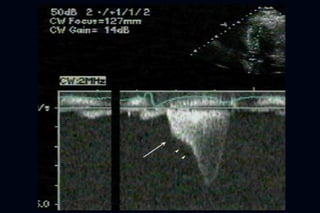
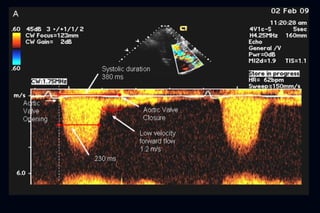
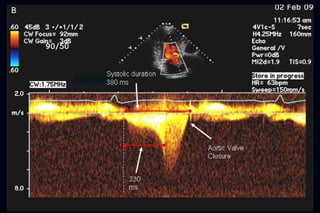
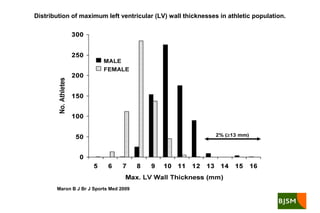
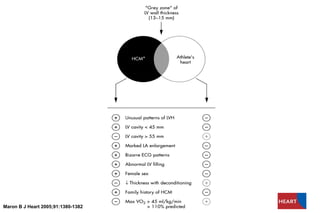
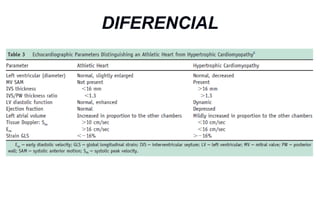
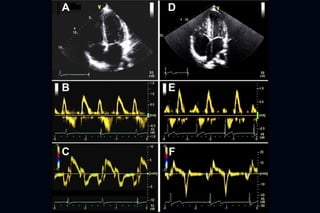
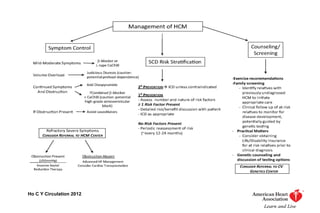
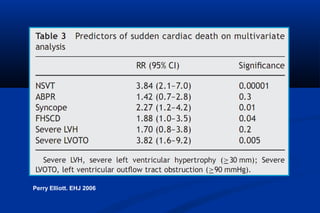
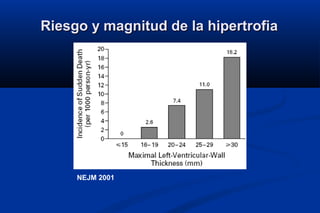
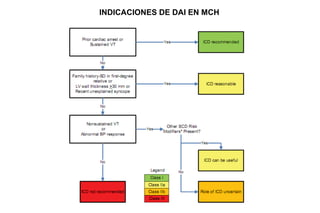
Este documento presenta información sobre la miocardiopatía hipertrófica (MCH), incluyendo su fisiopatología, hallazgos ecocardiográficos, diagnóstico diferencial y manejo. La MCH se caracteriza por una hipertrofia ventricular izquierda asimétrica que se debe a mutaciones genéticas. Puede causar obstrucción subaórtica y disfunción diastólica. El ecocardiograma muestra la hipertrofia septal típica. El tratamiento incluye bloqueadores beta para reducir