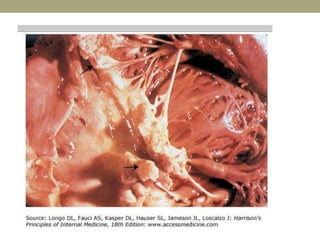
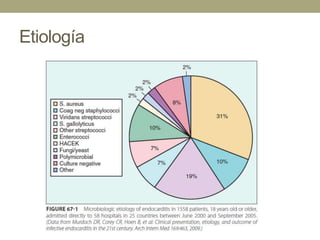
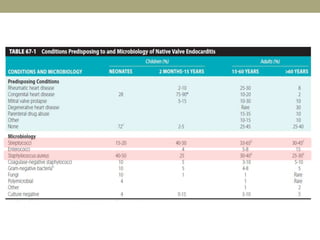
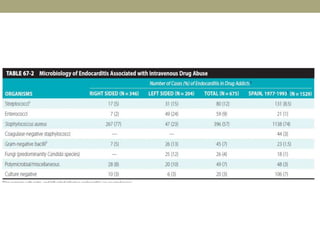
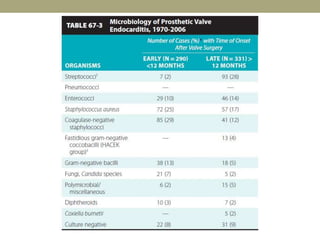
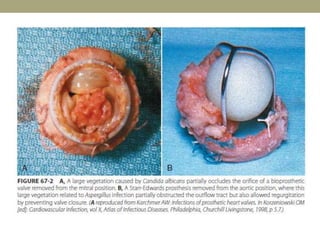
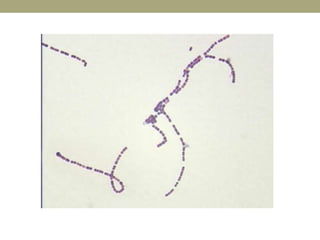
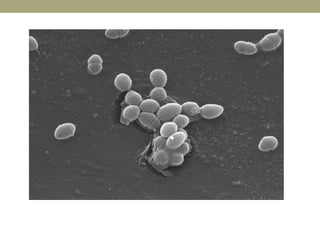
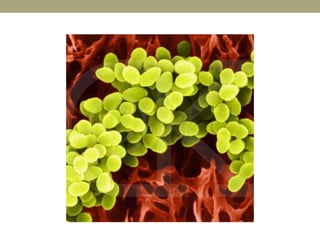
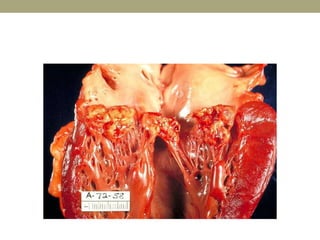
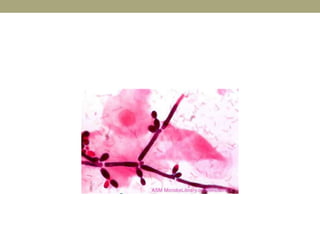
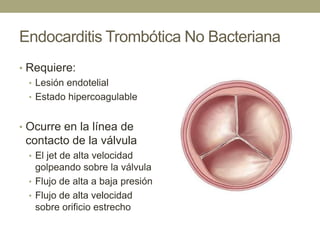
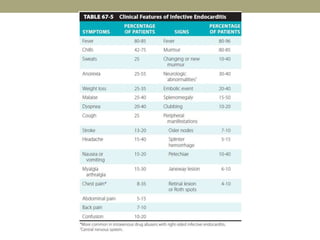
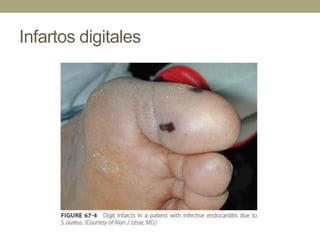
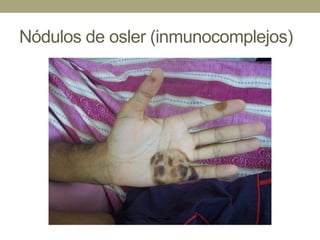
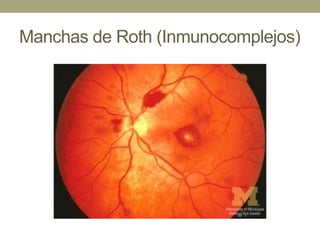
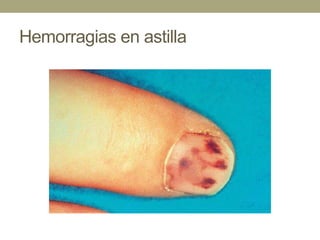
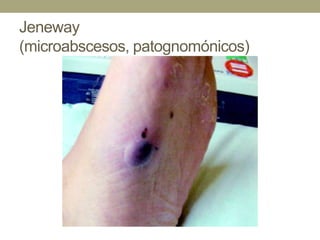
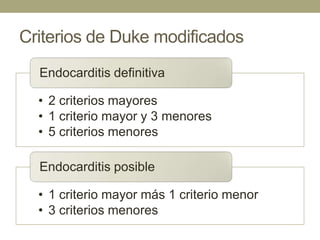
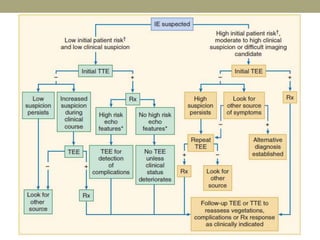
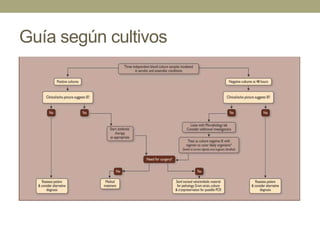
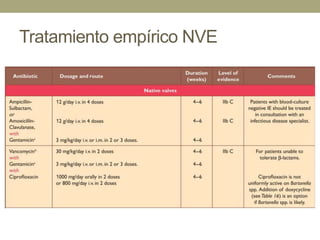
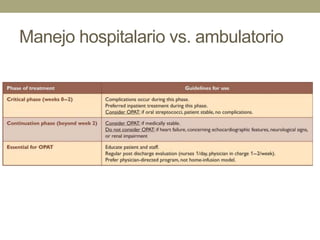
Este documento describe la endocarditis infecciosa, incluyendo su definición, epidemiología, etiología, fisiopatología, manifestaciones clínicas y enfoque diagnóstico. La endocarditis es una infección del endocardio que comúnmente afecta las válvulas cardíacas. Los principales microorganismos involucrados son estreptococos, estafilococos y enterococos. El diagnóstico se basa en criterios clínicos, ecocardiográficos y microbiológicos.