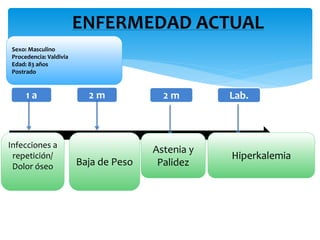
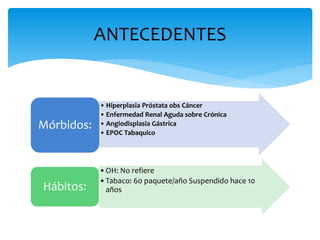
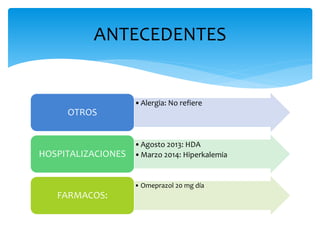
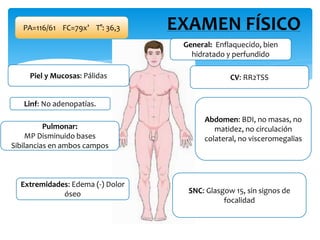
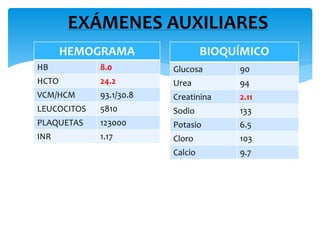
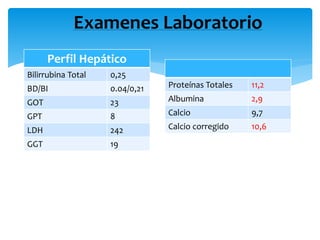
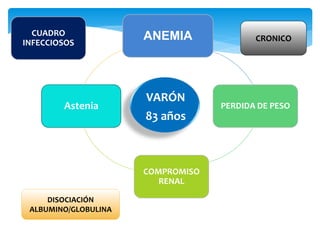
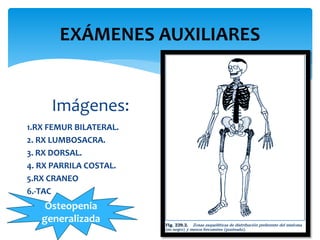
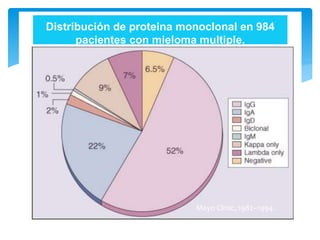
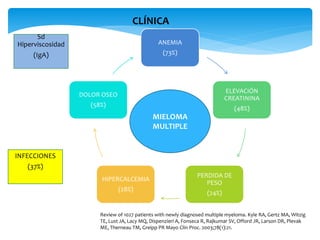
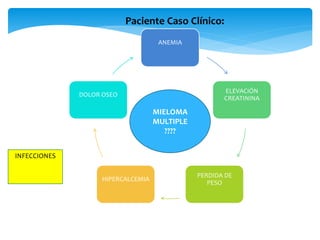
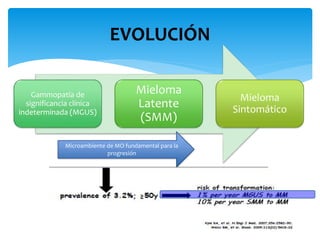
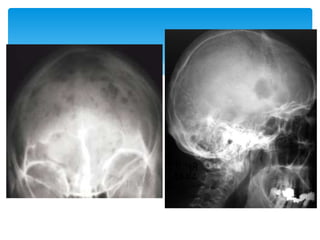
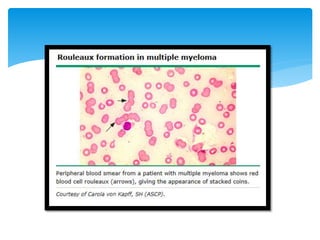
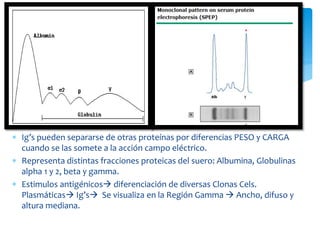
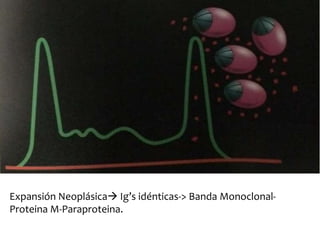
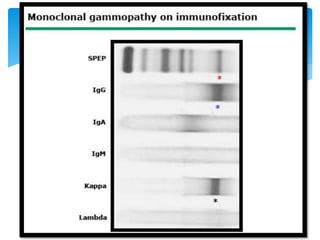
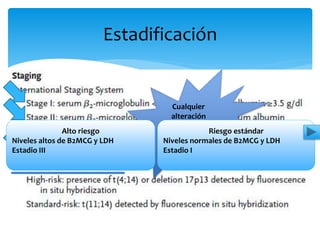
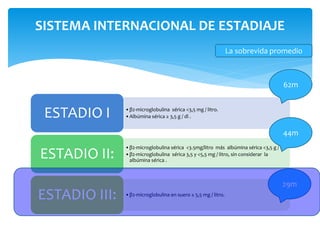
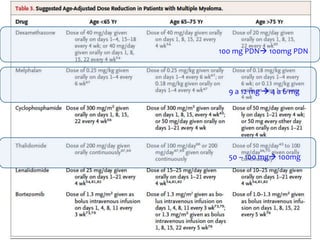
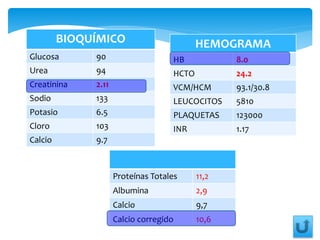
El documento presenta el caso clínico de un paciente de 83 años con mieloma múltiple. El paciente presentaba anemia, elevación de la creatinina, pérdida de peso y dolor óseo. Los exámenes auxiliares confirmaron el diagnóstico de mieloma múltiple IgA estadio IIIB. Se inició tratamiento con melfalán, prednisona y pamidronato.